Ny indikation - Svår kronisk rinosinuit med näspolyper (CRSwNP)1
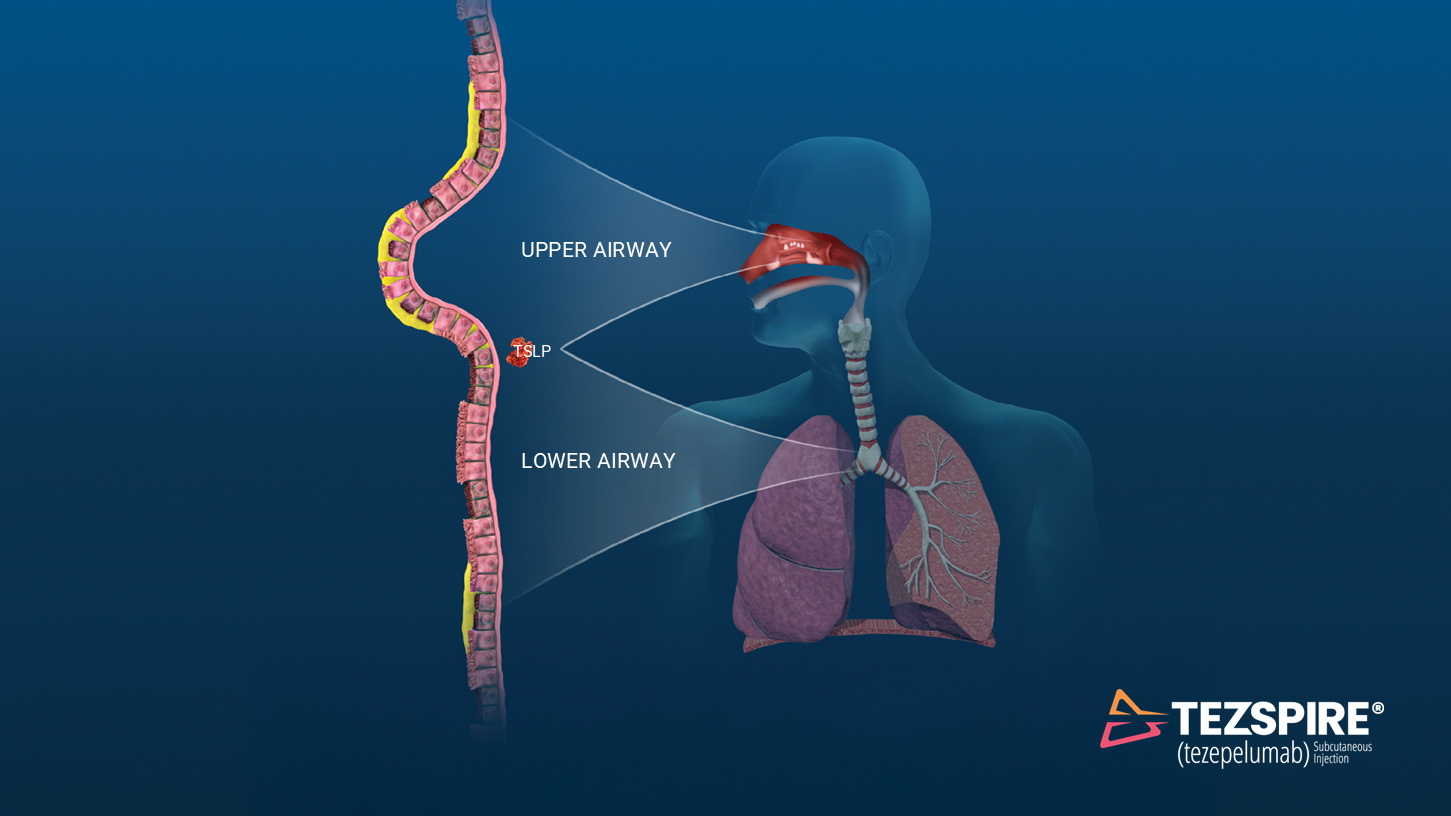
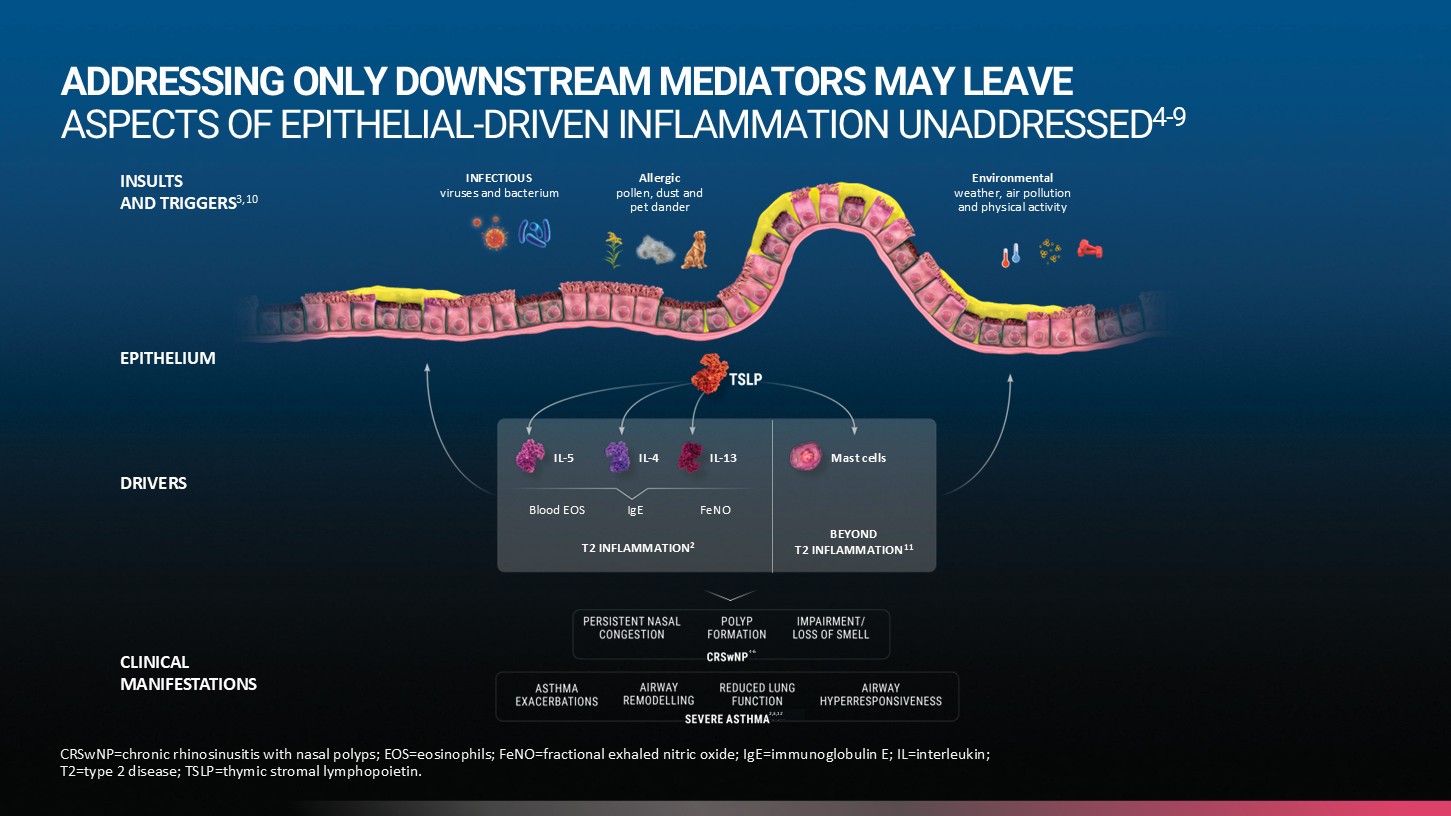
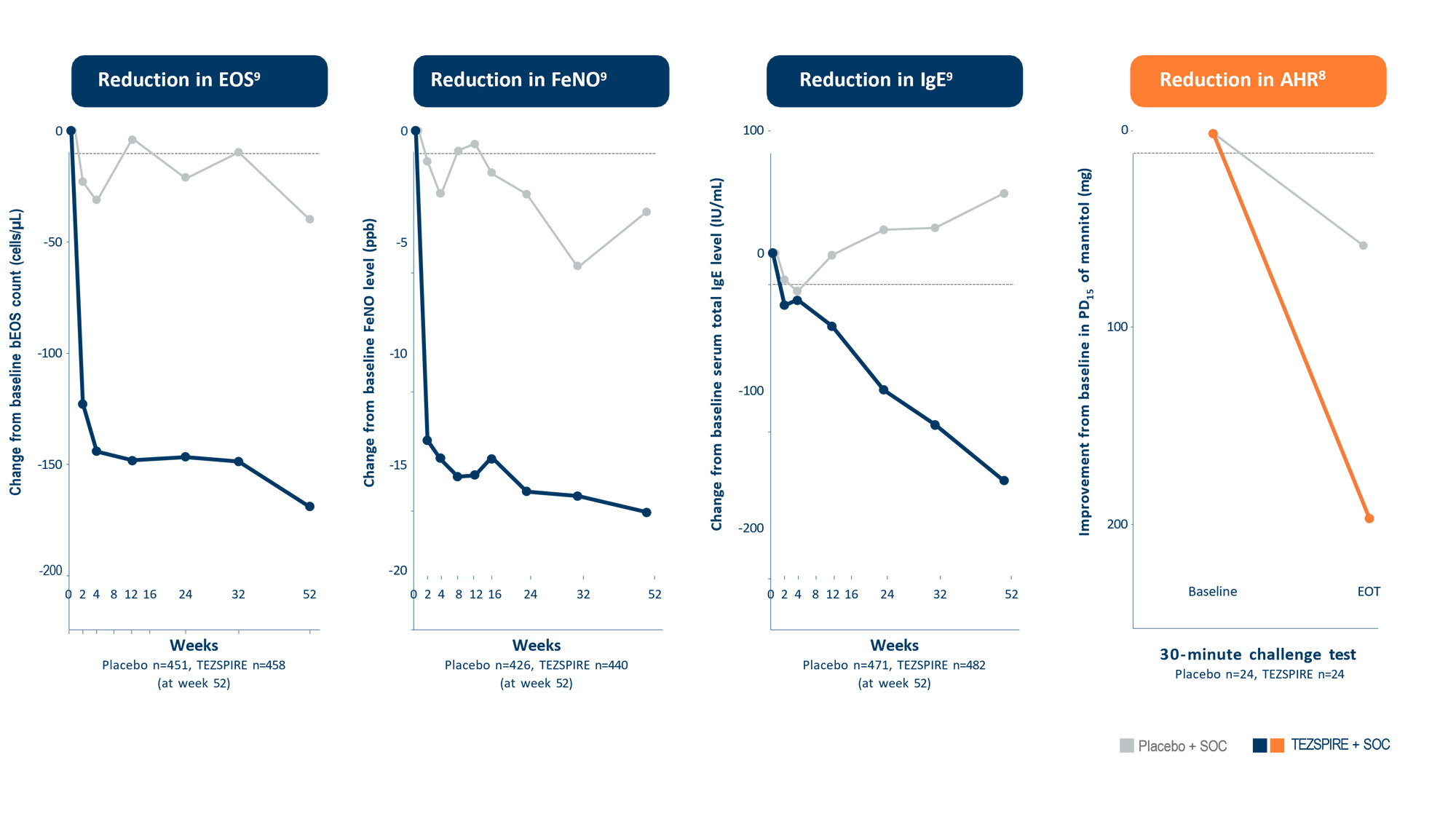
Tezspire är det första och enda läkemedel blockerar det epiteliala cytokinet TSLP (thymiskt stromalt lymfopoietin). Tezepelumab är en monoklonal antikropp som är riktad mot TSLP och hindrar interaktion med TSLP-receptorn. Blockering av TSLP med Tezspire reducerar nivån av ett brett spektrum av biomarkörer och cytokiner som förknippas med luftvägsinflammation såsom blodeosinofiler, eosinofiler i luftvägsslemhinnan, IgE, FeNO, IL‑5 och IL‑13.1
Tezspire har två godkända indikationer:
Kronisk rinosinuit med näspolyper1
Tezspire är indicerat för vuxna som tillägg till intranasala kortikosteroider för behandling vid svår kronisk rinosinuit med näspolyper hos patienter som inte uppnår tillräcklig sjukdomskontroll med systemiska kortikosteroider och/eller kirurgi.
Tezspire är inte subventionerat för svår kronisk rinosinuit med näspolyper.
Astma1
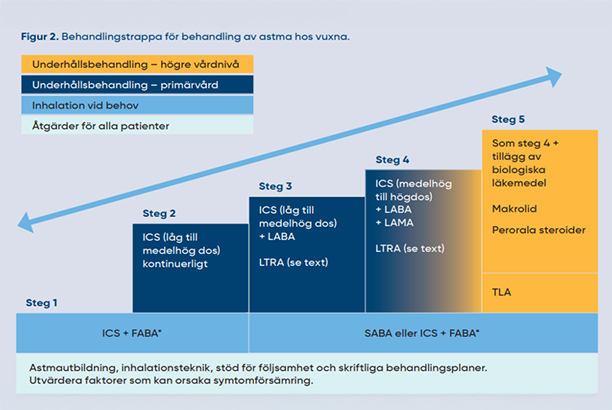
Tezspire är indicerat hos vuxna och ungdomar (12 år och äldre), som tillägg till underhållsbehandling vid svår astma som är otillräckligt kontrollerad trots högdos av inhalerade kortikosteroider plus ytterligare ett läkemedel som underhållsbehandling.
Tezspire subventioneras endast för patienter med otillräckligt kontrollerad astma trots underhållsbehandling med hög dos inhalationssteroider i kombination med ett annat läkemedel och som kännetecknas av förhöjda nivåer av eosinofiler och FeNO eller allergisk astma.