Lynparza (olaparib) Antineoplastiska läkemedel, övriga antineoplastiska läkemedel, PARP-hämmare. ATC-kod: L01XK01 Filmdragerade tabletter 100 och 150 mg. Rx.
Filmdragerade tabletter 100 och 150 mg.
Indikationer:
Äggstockscancer:
1) Lynparza tabletter är indicerade som monoterapi för underhållsbehandling av vuxna patienter med avancerad (FIGO stadie III och IV) BRCA1/2-muterad (nedärvd och/eller somatisk) höggradig epitelial ovarial-, tubar- eller primär peritonealcancer som är i respons (komplett eller partiell) efter avslutad första linjens platinumbaserad cytostatikabehandling. (F) = ingår i förmånen med begränsning, subventioneras vid ovanstående indikation.
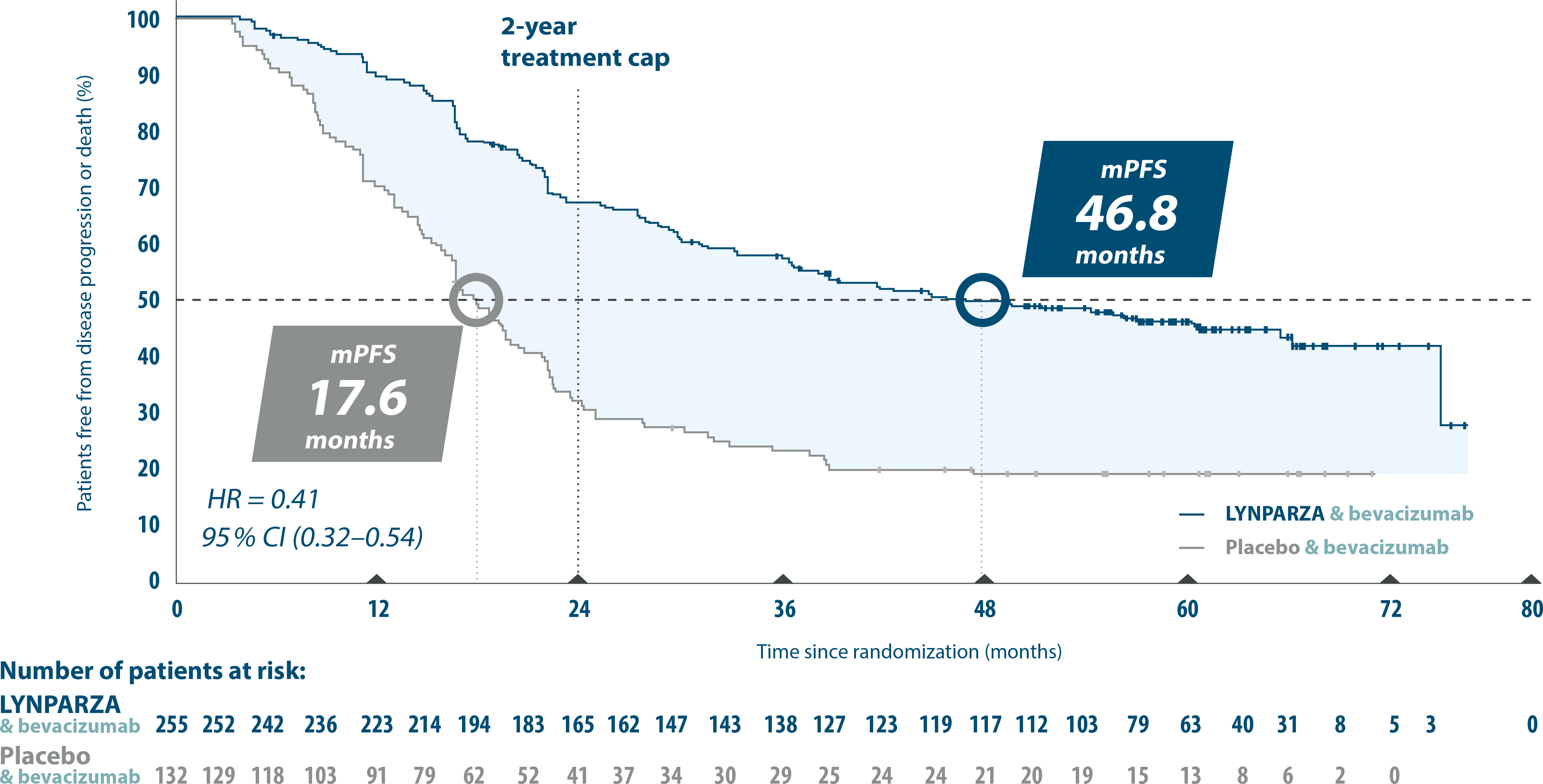
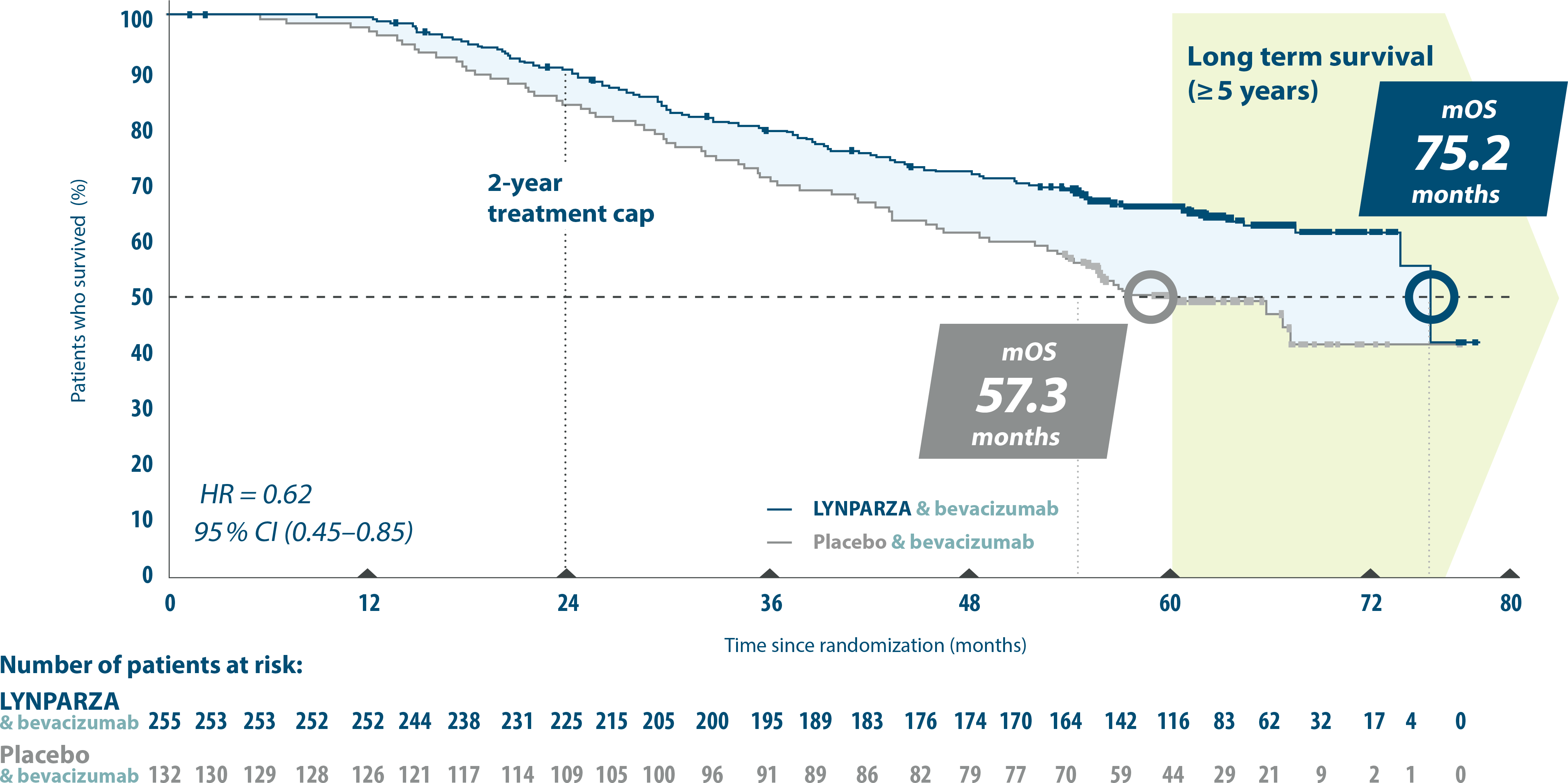
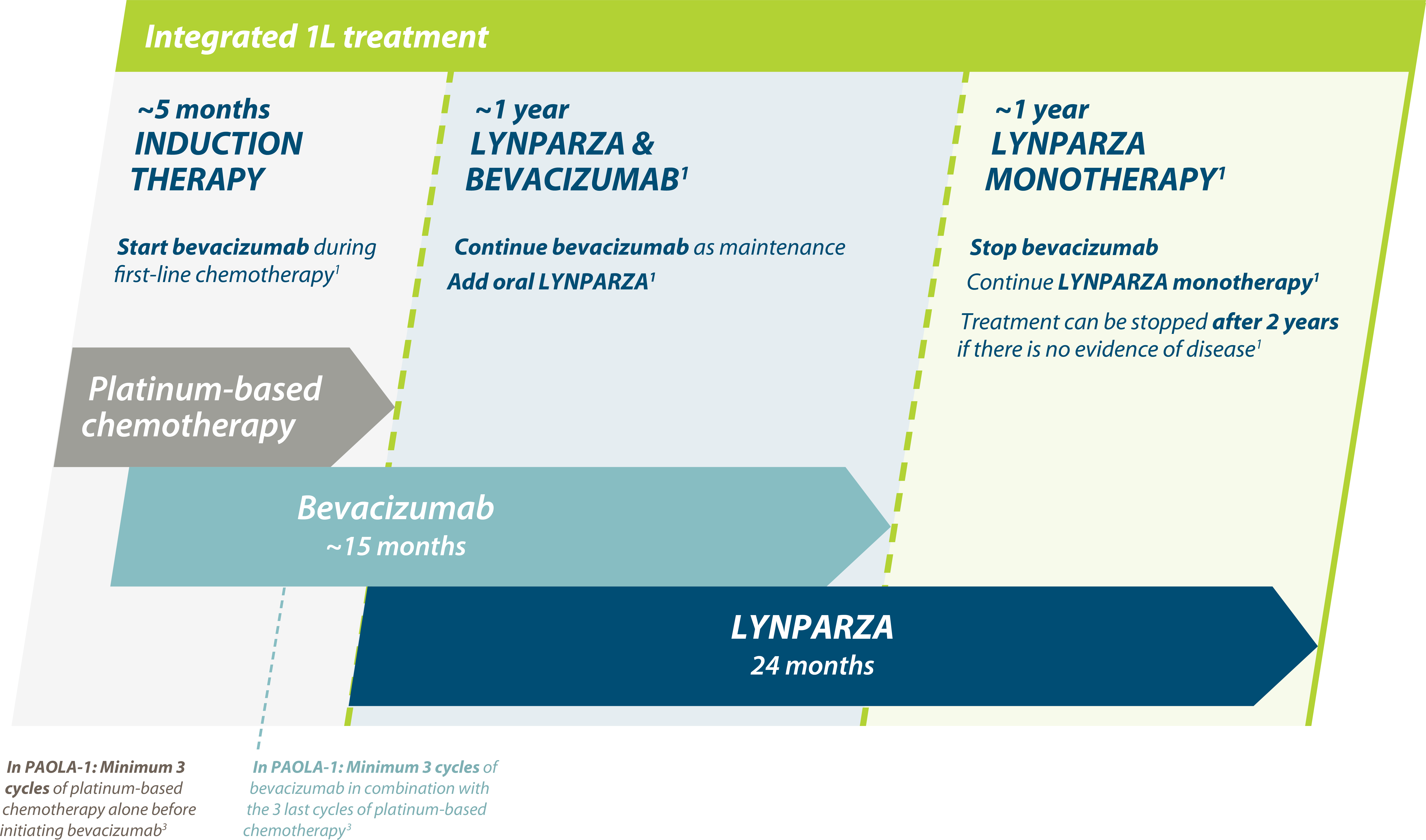
2) Lynparza tabletter i kombination med bevacizumab är indicerade som underhållsbehandling av vuxna patienter med avancerad (FIGO stadie III och IV) höggradig epitelial ovarial-, tubar- eller primär peritonealcancer som är i respons (komplett eller partiell) efter avslutad första linjens platinumbaserad cytostatikabehandling i kombination med bevacizumab och vars cancer är associerad med en positiv status för defekt homolog rekombination (HRD) som definieras antingen av en BRCA1/2-mutation och/eller genomisk instabilitet. (F) = ingår i förmånen med begränsning, subventioneras vid ovanstående indikation.
3) Lynparza tabletter är indicerade som monoterapi för underhållsbehandling av vuxna patienter med platinumkänslig recidiverande höggradig epitelial ovarial-, tubar- eller primär peritonealcancer och som är i respons (komplett eller partiell) efter platinumbaserad cytostatikabehandling. EF = Ingår inte i förmånen.
Dosering: Behandling med Lynparza ska initieras och övervakas av läkare med erfarenhet av cancerläkemedel.
Kontraindikationer: Överkänslighet mot den aktiva substansen eller mot något hjälpämne. Amning under behandlingen och 1 månad efter den sista dosen.
Varningar och försiktighet: Lynparza får inte användas under graviditet.
Hematologisk toxicitet: Provtagning vid initiering av behandlingen och därefter månatliga kontroller av fullständig blodstatus rekommenderas under de första 12 behandlingsmånaderna och därefter med jämna mellanrum. Om en patient får allvarlig hematologisk toxicitet eller är beroende av blodtransfusioner, ska behandlingen med Lynparza avbrytas och lämpliga blodtester göras.
Myelodysplastiskt syndrom/akut myeloisk leukemi: Om MDS/AML misstänks ska patienten remitteras till en hematolog för vidare utredning, inklusive benmärgsanalys och blodprovtagning för cytogenetik. Om MDS/AML bekräftas efter utredning avseende långvarig hematologisk toxicitet ska Lynparza sättas ut och patienten ska erhålla lämplig behandling.
Senaste översyn av Produktresumén: 20250605. För ytterligare information och priser se www.fass.se.
AstraZeneca AB, 151 85 Södertälje tel: 08 – 553 260 00. www.astrazeneca.se
SE-19682-08-25-ONC



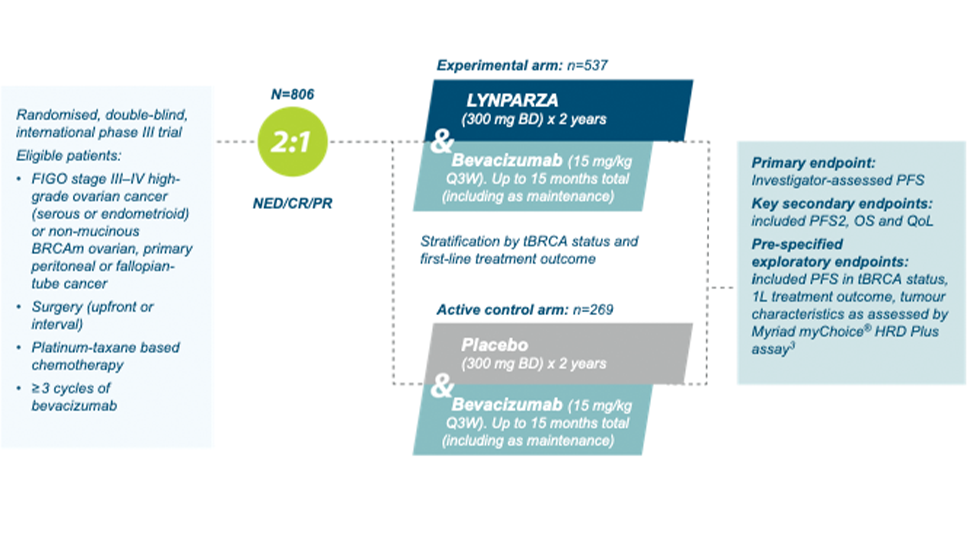 Figure created by AZ based on Ray-Coquard et al. (2019)2
Figure created by AZ based on Ray-Coquard et al. (2019)2