Hold deg oppdatert!
Få relevant informasjon om blant annet:
- Medisinske nyheter
- Webinarer
- Pasientstøtte
- Produktinformasjon
- Bivirkningsrapportering
Du kan når som helst trekke tilbake ditt samtykke.

Alvorlig astma
Lesetid: 6 min
Tezspire reduserer antall forverringer og bedrer lungefunksjonen, uavhengig av nivået på biomarkører og på tvers av fenotyper.1,2 Her får du en oversikt over studiedataene for Tezspire.2-4
Tezspire er studert i to fase II-studier og én fase III-studie, med til sammen 1727 pasienter med ukontrollert og/eller alvorlig astma.2-4
Videoforedrag om studiene - spørsmål og svar på 8 minutter. Se lege og forsker Sigrid Vikjord presentere effektdataene fra studiene med Tezspire.
Framtil nå har vi ikke sett noen medikamenter som har klart å blokkere denne type inflammasjon1,2
Sigrid Vikjord. lege og forsker St Olav og NTNU
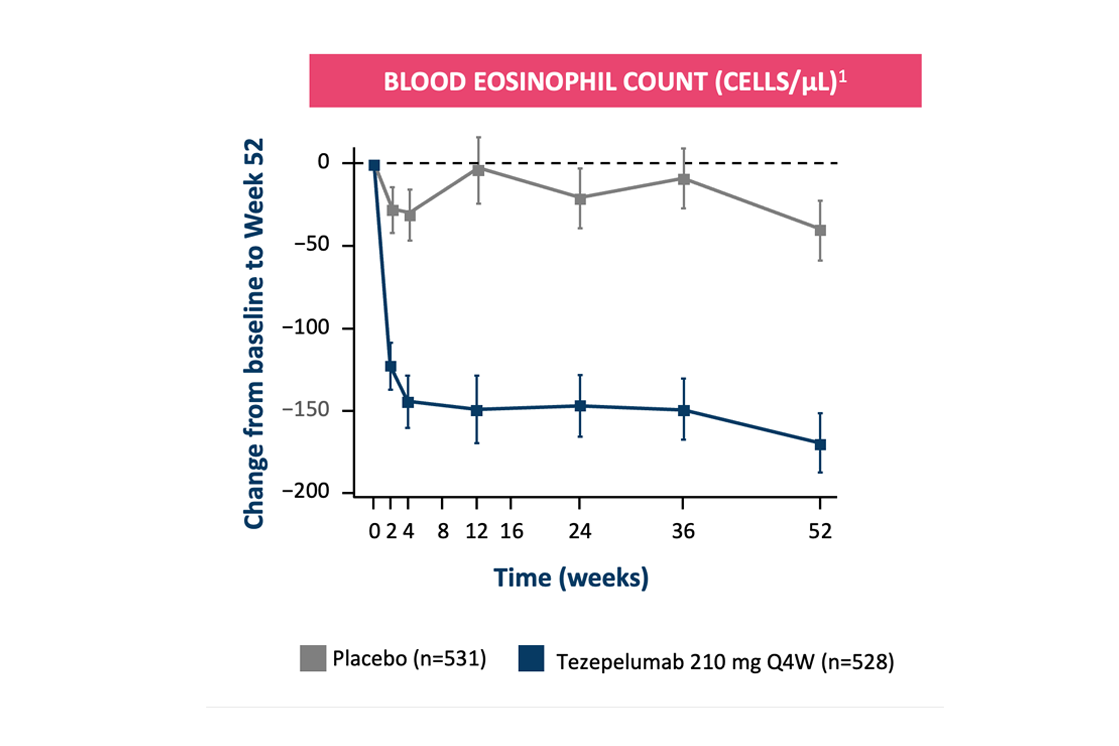
Nedgang i eosinofiler i blodet
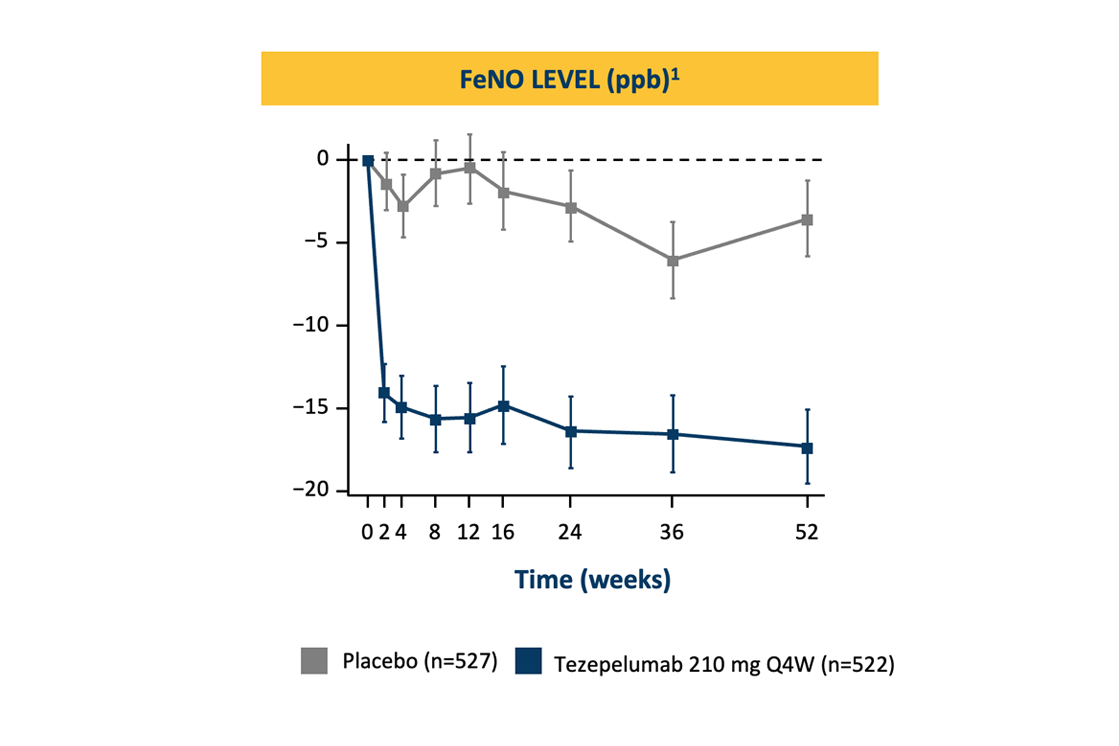
Redusert FeNO-nivå (ppb)
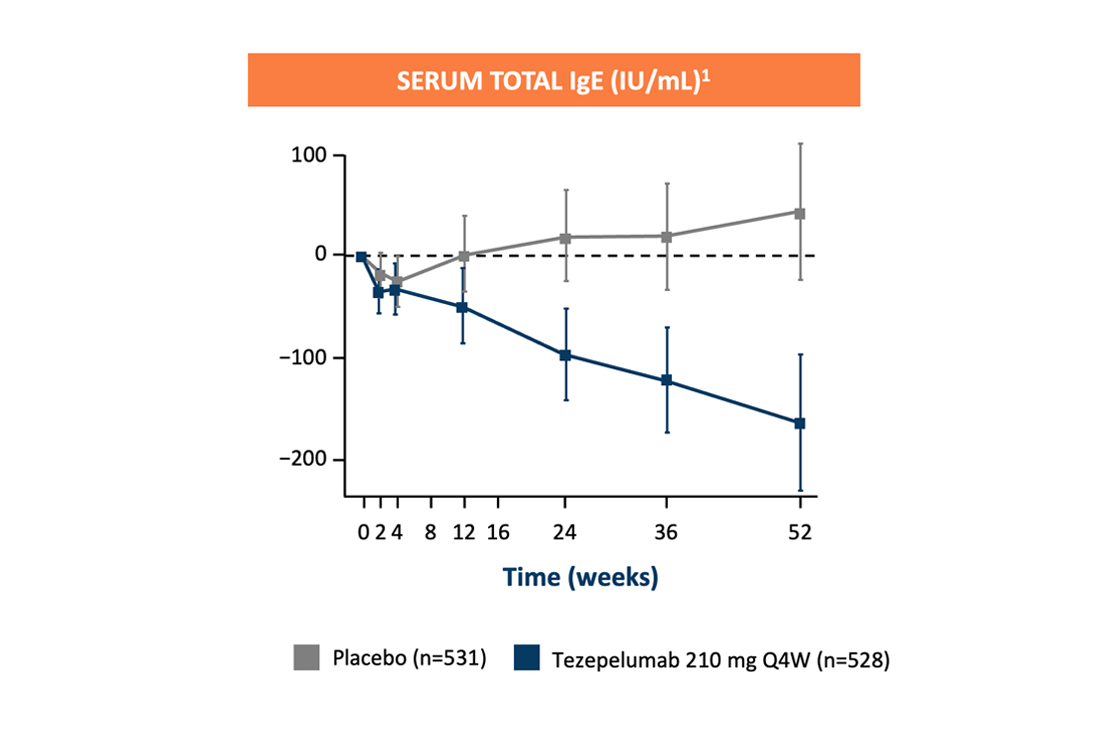
Mindre IgE i serum
Reduksjon EOS4
Det primære endepunktet i Cascade var å studere reduksjonen av eosinofiler i lungevev, fra baseline til studieslutt. For pasienter som fikk Tezpire var reduksjonen 89 %, mens for pasienter som fikk placebo var den 25 %, altså 6,7 ganger større reduksjon til fordel for Tezspire (p<0,001).4
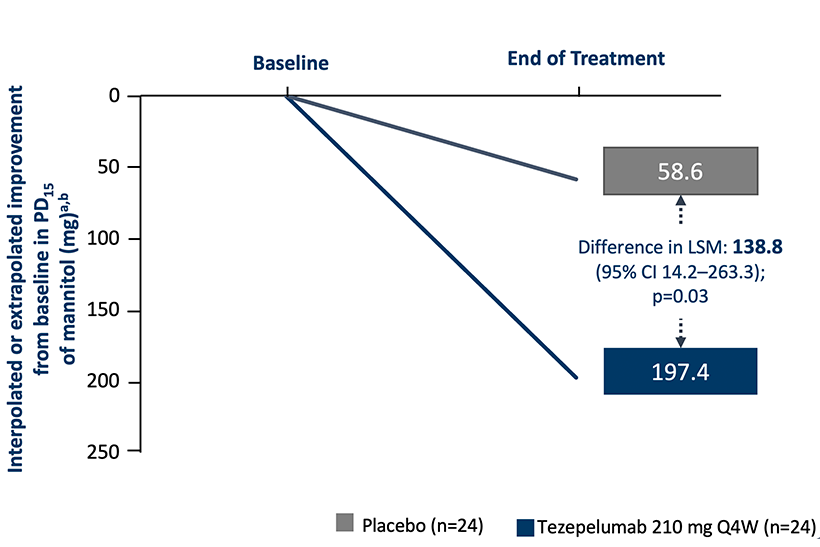
Redusert hyperreaktivitet
Hyperreaktivitet i luftveiene ble testet via en provokasjonstest med mannitol.4 PD15 er den dosen mannitol som er nødvendig for å gi en 15 % reduksjon i FEV(1) fra baseline. Jo høyere PD15 er, desto lavere er luftveienes hyperreaktivitet.
I studien ble det sett en større reduksjon i hyperreaktivitet i luftveiene etter behandling med Tezspire enn det som ble observert i placebo-gruppen.4 Beregninger av effekten av Tezspire på hyperreaktivitet i luftveiene er basert på mekanistiske studier, og den kliniske signifikansen av dette resultatet er derfor ikke fastslått.
AAER=annual asthma exacerbation (årlig astmaforverring)
CI=confidence interval (konfidensintervall)
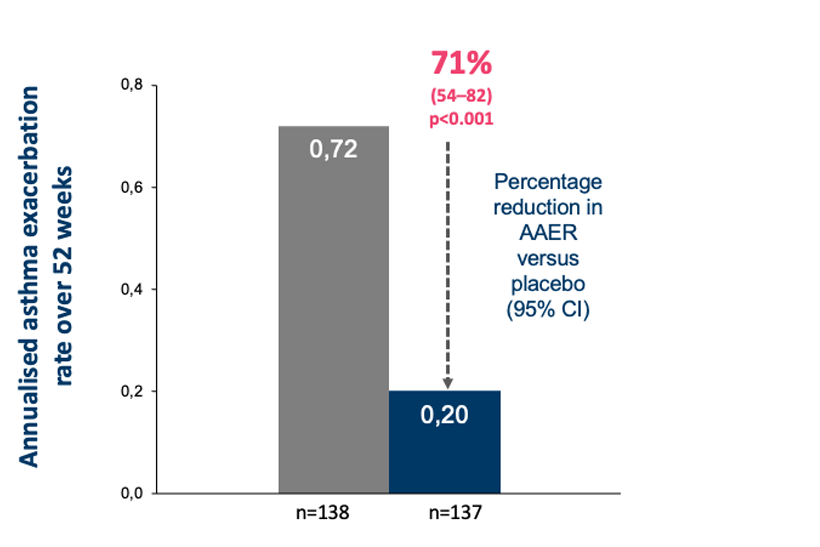
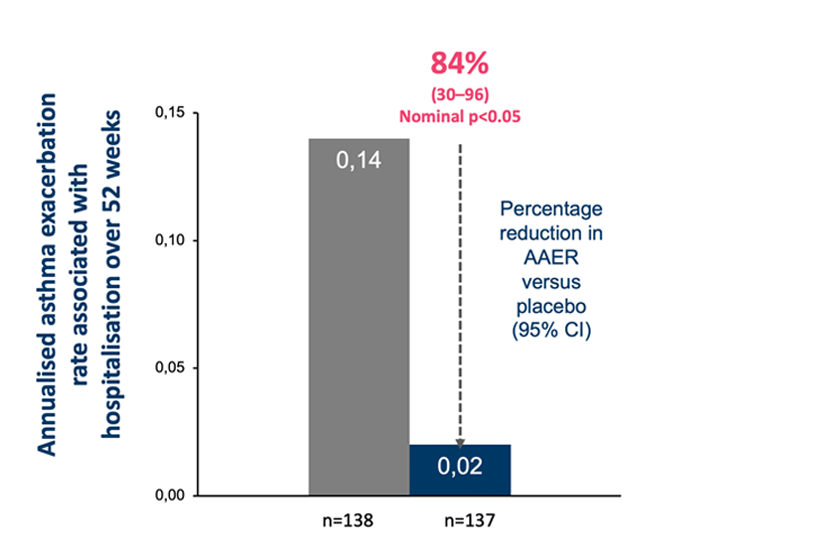
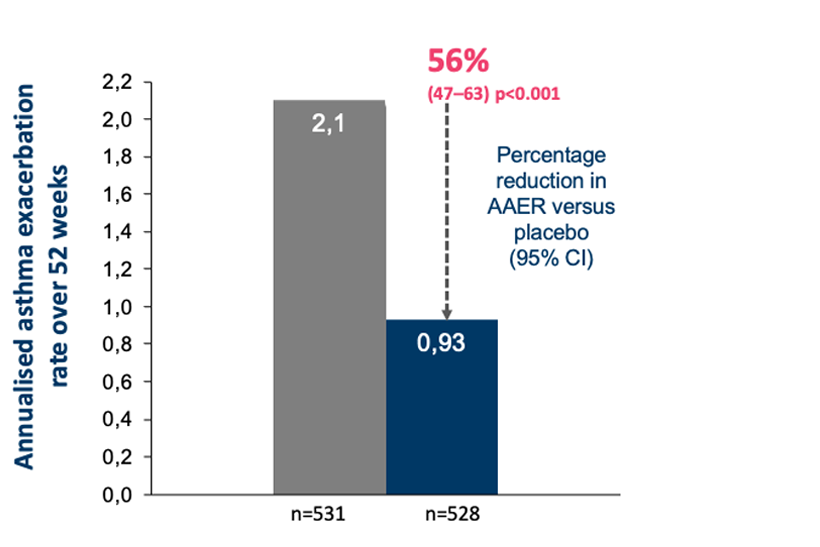
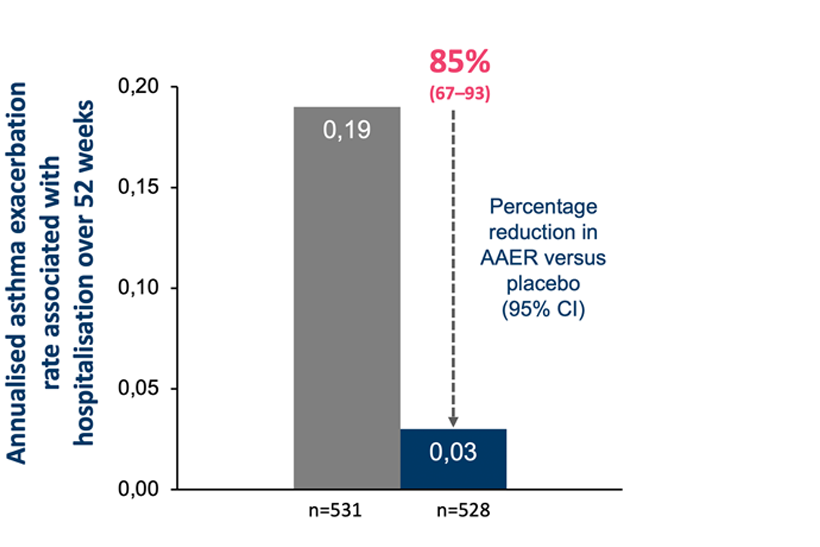
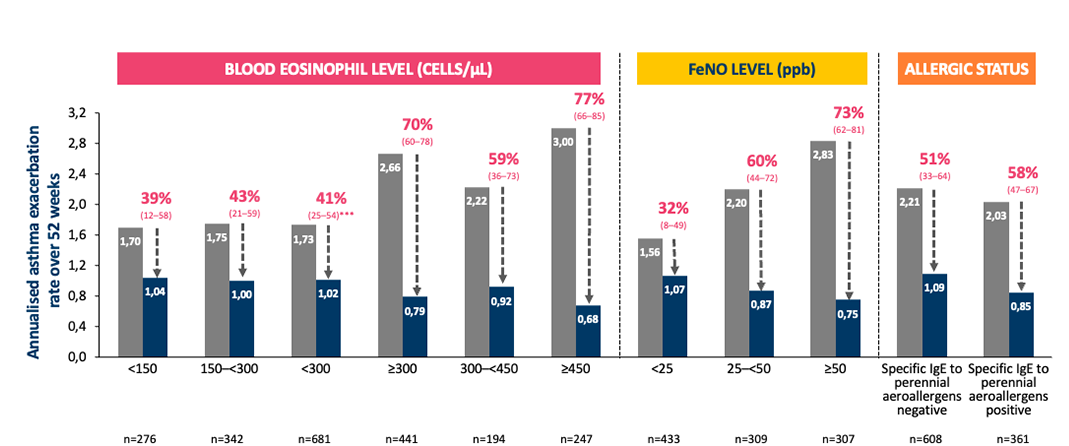
Navigator er en av de to pivotale registreringsstudiene som så på effekt og sikkerhet til Tezspire. Det primære endepunktet var årlig frekvens av astmaeksaserbasjoner og studien gikk over 52 uker.3
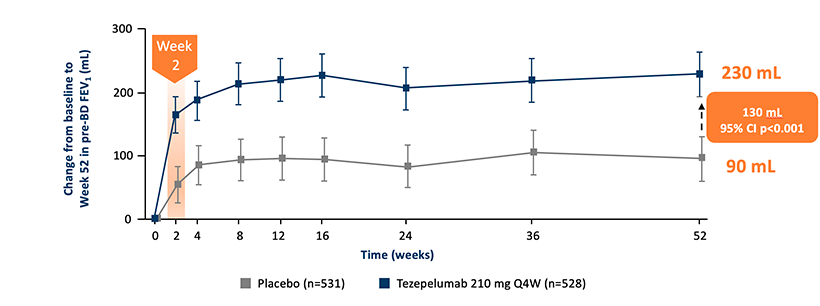
Forbedring av lungefunksjon (pre-BD-FEV1) etter bare to uker.3
MCID= minimum clinically important difference (minste kliniske viktige forskjell)
LS=Least Square, pre-BD FEV1= forced expiratory volume in 1 second (pre-bronkodilator forsert ekspiratorisk verdi ved 1 sekund), CI=confidence interval (konfidensintervall)
ACQ – asthma control questionnaire (astmakontrollspørreskjema)
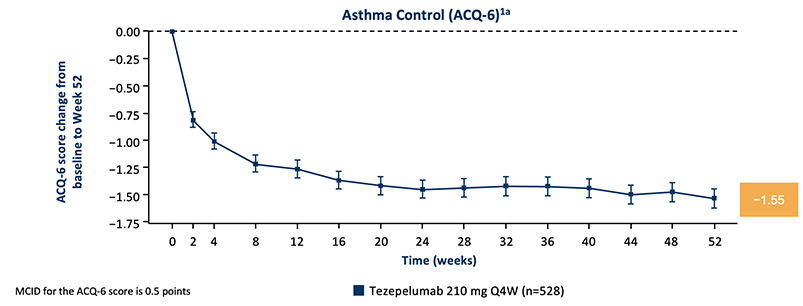
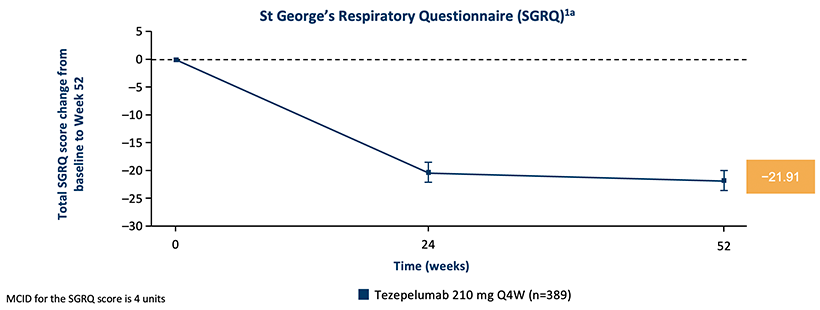
I studiene ble det ikke rapportert klinisk signifikant flere bivirkninger hos de pasientene som ble behandlet med Tezspire enn hos placebo-gruppene.2,3
Se lege og forsker Sigrid Vikjord presentere effektdataene fra studiene med Tezspire.
Det er gjort flere studier som viser god effekt av Tezspire sammenlignet med en gruppe som får placebo-medisin. Det man ser primært er at Tezspire har færre forverringer av astma i løpet av år, men også betydelig effekt på blant annet lungefunksjon, økt lungefunksjon tidlig i behandlingsforløpet og reduksjon i typiske betennelsemarkører i blodet2-5
Sigrid Vikjord. lege og forsker St Olav og NTNU
Indikasjon:6 Tezspire er indisert som tillegg til vedlikeholdsbehandling hos voksne og ungdom i alderen 12 år og eldre med alvorlig astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
Vanlige bivirkninger:7 Faryngitt, utslett, artralgi, reaksjon på injeksjonsstedet.
Forsiktighetsregler:8 Skal ikke brukes til å behandle akutte astmaeksaserbasjoner. Astmarelaterte symptomer eller eksaserbasjoner kan oppstå. Pasienten bør instrueres om å oppsøke lege hvis astmaen forblir ukontrollert eller forverres. Brå seponering av kortikosteroider etter behandlingsoppstart anbefales ikke.
Dosering:9 Voksne (inkl. eldre) og ungdom ≥12 år 210 mg som s.c. injeksjon hver 4. uke. Til langtidsbehandling. Behovet for fortsatt behandling bør vurderes minst 1 gang årlig, basert på pasientens nivå av astmakontroll.

Vårt interaktive kasuistikkprogram for lungemedisin er ideelt for å skape engasjement og diskusjon for stille diagnose og velge behandling.
Kontakt Tor Sortåsløkken eller Silje Alsterberg
Ta kontakt for et diskusjonsmøte, vi tar gjerne med publikasjonene.
Kontakt Tor Sortåsløkken eller Silje Alsterberg
Behandlingsmålet ved alvorlig astma er likt som hos andre personer med astma: Normal lungefunksjon...
Les mer
Den kliniske kompleksiteten ved alvorlig astma, som også gir utfordringer med behandling, finner no...
Les merIndikasjon: Astma: Tezspire er indisert som tillegg til vedlikeholdsbehandling hos voksne og ungdom i alderen 12 år og eldre med alvorlig astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
Kronisk rhinosinusitt med nesepolypper (CRSwNP): Tezspire er indisert som tillegg til behandling med intranasale kortikosteroider hos voksne pasienter med alvorlig CRSwNP der behandling med systemiske kortikosteroider og/eller kirurgi ikke gir tilstrekkelig sykdomskontroll.
Dosering: Astma: Voksne og ungdom (fra 12 år og eldre) Den anbefalte dosen er 210 mg tezepelumab som subkutan injeksjon hver 4. uke.
CRSwNP: Den anbefalte dosen for voksne pasienter er 210 mg tezepelumab som subkutan injeksjon hver 4. uke.
Forsiktighetsregler: Skal ikke brukes til å behandle akutte astmaeksaserbasjoner. Astmarelaterte symptomer eller eksaserbasjoner kan oppstå. Pasienten bør instrueres om å oppsøke lege hvis astmaen forblir ukontrollert eller forverres. Alvorlige infeksjoner bør behandles før oppstart av behandling. Ved utvikling av alvorlig infeksjon under behandling, bør behandlingen seponeres inntil denne er over. Graviditet og amming: Bruk under graviditet bør unngås med mindre forventet nytte for den gravide oppveier mulig risiko for fosteret.
Vanlige bivirkninger: Faryngitt, utslett, artralgi, reaksjon på injeksjonsstedet.
Pakninger og priser: Injeksjonsvæske, oppløsning i ferdigfylt penn (210 mg): 1 stk: kr. : 15 053,40. Injeksjonsvæske, oppløsning i ferdigfylt sprøyte (210 mg): 1 stk. kr. : 15 053,40.
Reseptgruppe: C. Refusjon: H-resept. Refusjonsberettiget bruk: Vilkår: 216 Refusjon ytes kun etter resept fra sykehuslege eller avtalespesialist. Der det er utarbeidet nasjonale handlingsprogrammer/nasjonal faglig retningslinje og/eller anbefalinger fra RHF/LIS spesialistgruppe skal rekvirering gjøres i tråd med disse Tezspire inngår i RHF anbefalinger for alvorlig ukontrollert T2-høy astma.
Beslutning i Beslutningsforum for nye metoder 18.03.2024. Tezepelumab (Tezspire) innføres som tillegg til vedlikeholdsbehandling ved alvorlig astma med eosinofili hos voksne og ungdom i alderen 12 år og eldre som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
Beslutning i beslutningsforum for nye metoder 19.01.2026. Tezspire (tezepelumab) innføres som tillegg til behandling med intranasale kortikosteroider hos voksne pasienter med alvorlig CRSwNP der behandling med systemiske kortikosteroider og/eller kirurgi ikke gir tilstrekkelig sykdomskontroll.
For fullstendig informasjon, les mer på www.felleskatalogen.no
AstraZeneca AS - www.astrazeneca.no – P. box 6050 Etterstad - 0601 Oslo
ID: NO-15164-01-2026-TEZ
Tezspire SPC 5.1.
Corren J, Parnes JR, Wang L et al. Tezepelumab in Adults with Uncontrolled Asthma. N Engl J Med. 2017;377:936-46.
Menzies-Gow A, Corren J, Bourdin A et al. Tezepelumab in Adults and Adolescents with Severe, Uncontrolled Asthma Supplementary information. N Engl J Med. 2021;384:1800-9.
Diver S, Khalfaovi L, Emson C et al. Effect of tezepelumab on airway inflammatory cells, remodelling, and hyperresponsiveness in patients with moderate-to-severe uncontrolled asthma (CASCADE): a double-blind, randomised, placebo-controlled, phase 2 trial. Lancet Respir Med. 2021;9:1299-1312.
Corren J, Chen S, Callan Let al. The effect of tezepelumab on hospitalizations and emergency department visits in patients with severe asthma. Ann Allergy Asthma Immunol. 2020;125:211-14.
Tezspire SPC 4.1.
Tezspire SPC 4.8
Tezspire SPC 4.4.
Tezspire SPC 4.2
Tezspire på felleskatalogen.no