
PAOLA-1
LYNPARZA (olaparib) in combination with bevacizumab for HRD-positive patients with advanced ovarian cancer. 1
PAOLA-1 study
Katharina Bischof, MD, PhD Senior Consultant at Radiumhospitalet, Oslo University Hospital, talks about the PAOLA-1 study and the Norwegian recommendations for primary maintenance treatment for advanced high-grade serous ovarian cancer.
LYNPARZA + bevacizumab for HRD-positive patients with advanced ovarian cancer2
PAOLA-1 was a randomized, double-blind, phase III trial conducted in 11 countries. It evaluated maintenance therapy with Lynparza + bevacizumab, compared with placebo + bevacizumab, in patients with newly diagnosed advanced ovarian cancer, irrespective of biomarker or surgical status, who were in clinical response after first-line platinum-based chemotherapy plus bevacizumab.2
Why combine LYNPARZA with bevacizumab?
Multiple cell populations exist in the same tumor already at diagnosis, and it has strong clinical implications. Consequently, single targeted agents may not effectively kill all tumor cells and different targeted agents need to be combined to collectively act through inhibition of distinct pathways.3
PARP inhibitors, such as LYNPARZA, provoke tumor cell death by inducing DNA double-strand breaks in the cells with homologous recombination deficiency (HRD; read more about HRD as a biomarker here).4 VEGF inhibitors such as bevacizumab, inhibit angiogenesis and thus tumor growth through the inhibition of the VEGF pathway.3 Preclinical studies have shown synergistic effects of PARP inhibitors and anti-angiogenic agents (e.g. bevacizumab). PARP inhibition is also shown to reduce VEGF expression and anti-angiogenic agents induce HRD. Therefore, the premise of combining LYNPARZA and bevacizumab is based on the rationale that direct targeting of PARP by LYNPARZA and indirect inhibition of homologous recombination by bevacizumab will be therapeutically beneficial compared to LYNPARZA or bevacizumab alone.4
LYNPARZA+bevacizumab provides long-term data on both PFS and OS for HRD-positive patients in exploratory subgroup analyses1,5
A statistically significant progression-free survival (PFS) benefit was demonstrated in the intention-to-treat (ITT) population with addition of Lynparza to bevacizumab vs placebo+bevacizumab. 2
Effect on OS and PFS were investigated in prespecified exploratory subgroup analyses in patients with BRCA1 and/or BRCA2 mutations and in those who tested positive for homologous recombination deficiency (HRD defined as a tumor BRCAm and/or genomic instability). The data showed a numerical improvement of OS and PFS with Lynparza+bevacizumab vs placebo+bevacizumab.1,5
PAOLA-1 study assessed LYNPARZA + bevacizumab efficacy in 1L maintenance setting using an active comparator arm 2
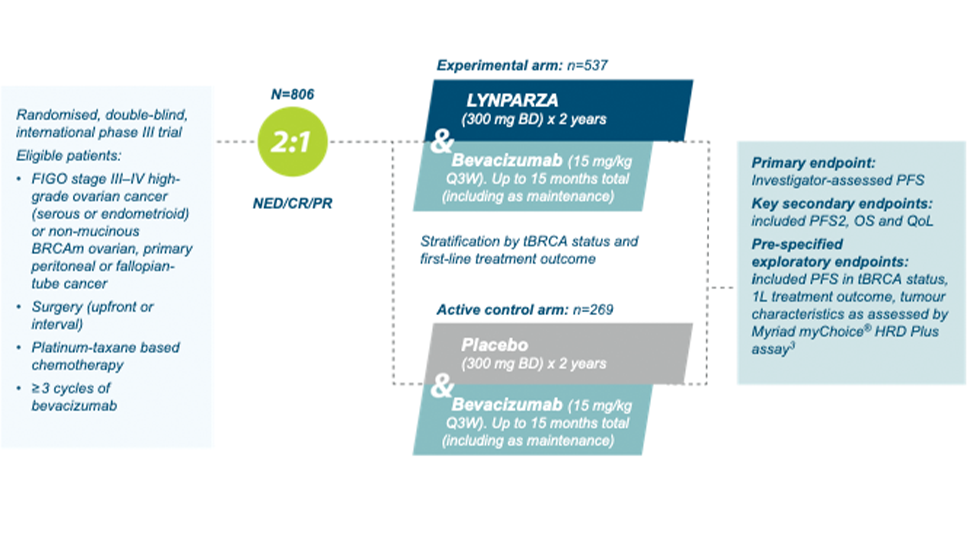
Figure created by AZ based on Ray-Coquard et al. (2019)2
PAOLA-1. 5 year pre-specified exploratory subgroup analysis:
PFS in HRD-positive patients5
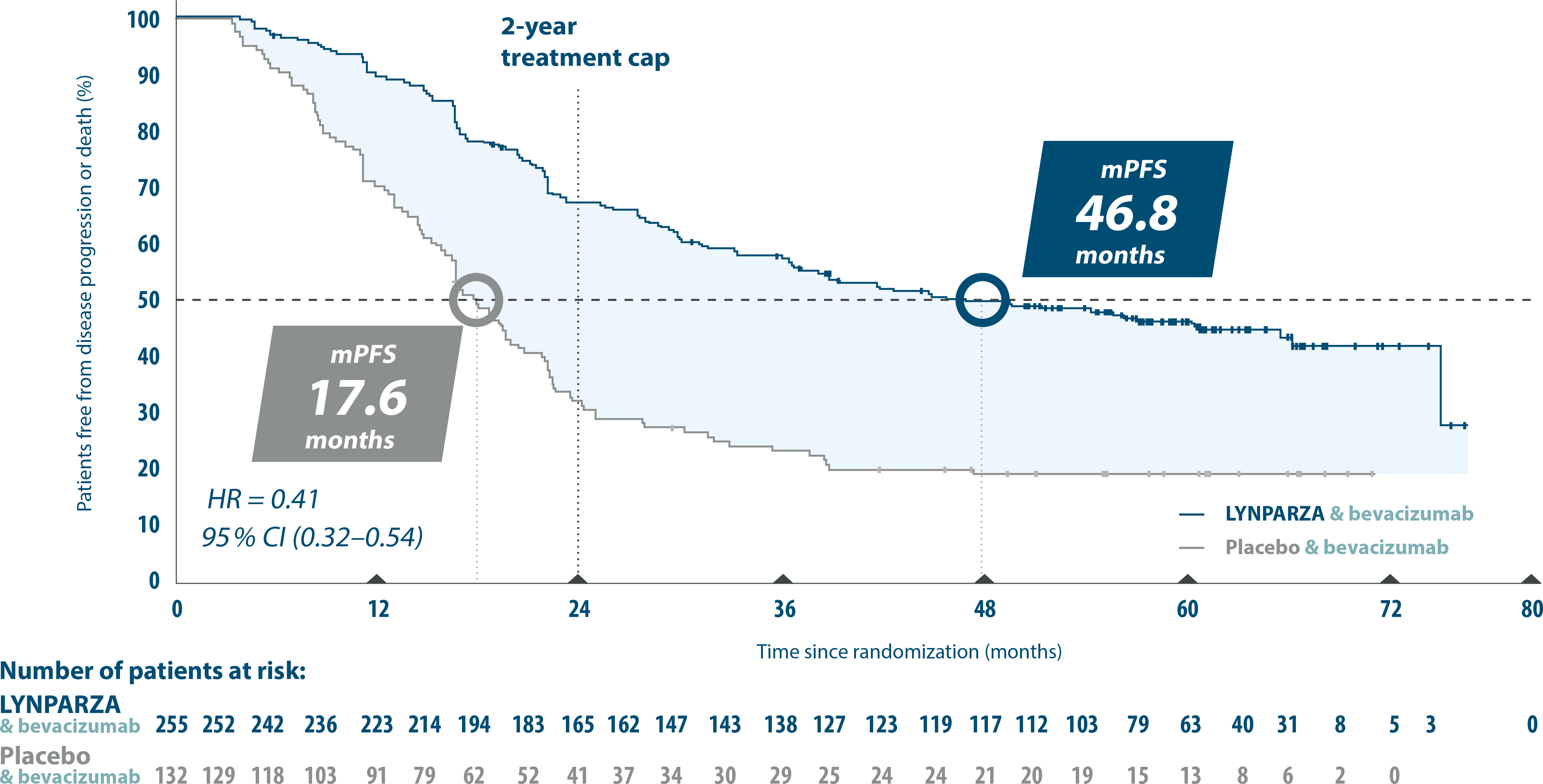
Adapted from Ray-Conquard, et al. 20235
Almost 4 years mPFS for patients treated with LYNPARZA+bevacizumab vs bevacizumab+pacebo (46.8 vs 17.6 months with placebo+bevacizumab. (HR 0.41, 95% Cl 0.32-0.54)5
PAOLA-1. 5 year pre-specified exploratory subgroup analysis:
Final OS in HRD-positive patients1,5
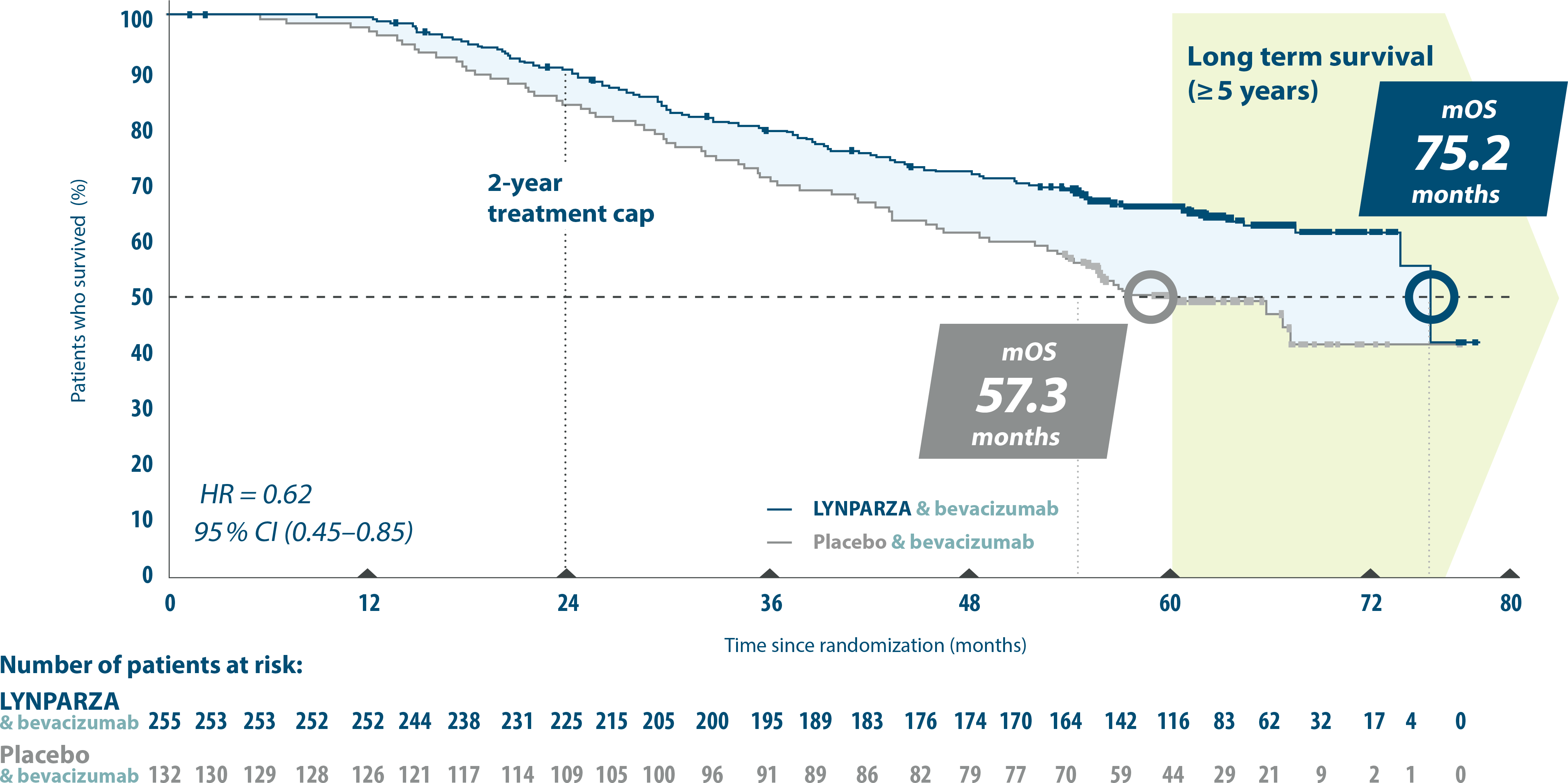
Adapted from Ray-Coquard, et al. 20235
6 years mOS at 5 years with LYNPARZA & bevacizumab vs placebo & bevacizumab (HR=0.62. 95% Cl 0.45-0.85).1,5
Patients receiving a PARPi during any subsequent treatment: LYNPARZA + bevacizumab 17.3 % vs placebo+ bevacizumab 50.8%.5
Read the whole publication now at sciencedirect.com
Assessing the impact of clinical risk on outcomes with LYNPARZA & bevacizumab8
All patients with advanced ovarian cancer are at high risk of disease progression6
- However, it is well known that disease stage and surgical outcome impact the risk of relapse and survival.7
- Even ”low-risk” group has a high risk of progression6
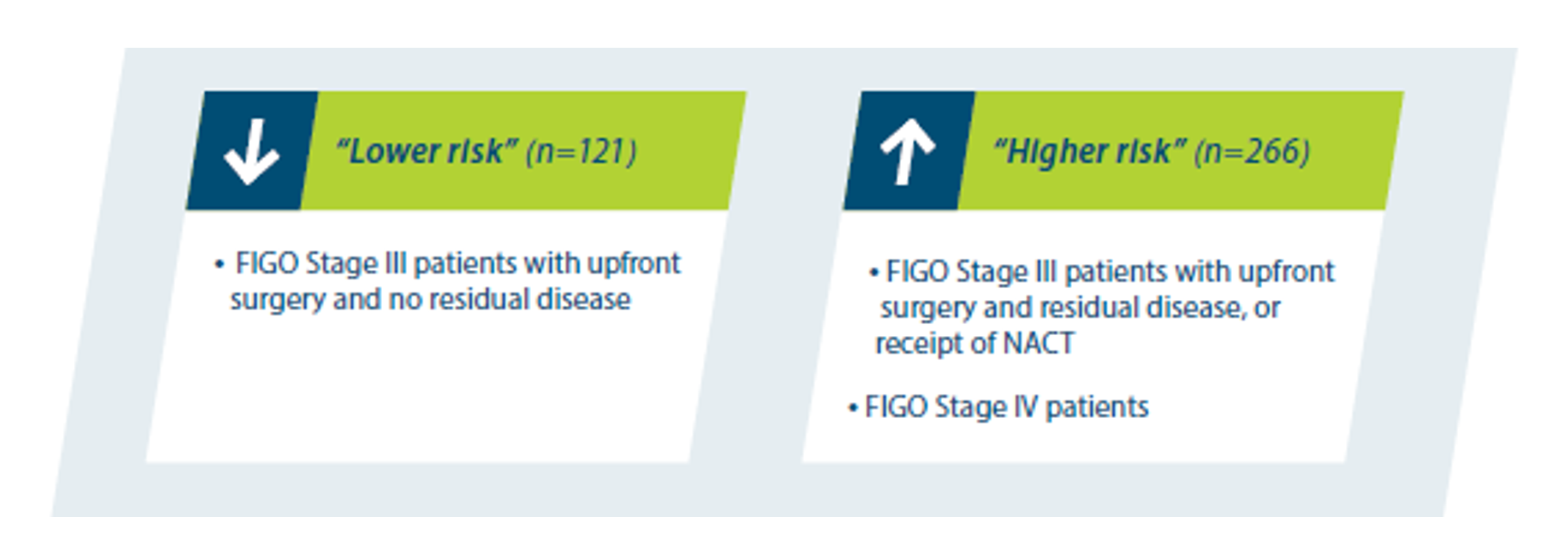
- Exploratory post-hoc analyses were performed to answer the question of how these factors may affect outcomes with LYNPARZA + bevacizumab.8
- The first analyzed PFS using data from the PAOLA-1 2-year primary analysis, and the second analyzed OS using data from the PAOLA-1 5-year OS analysis.8
LYNPARZA & bevacizumab improves both PFS and OS9
~1 of 2 patients were still alive at 5 years in ”higher risk” group9
5 year pre-specified exploratory subgroup analysis: HRD-positive patients ”higher risk*”
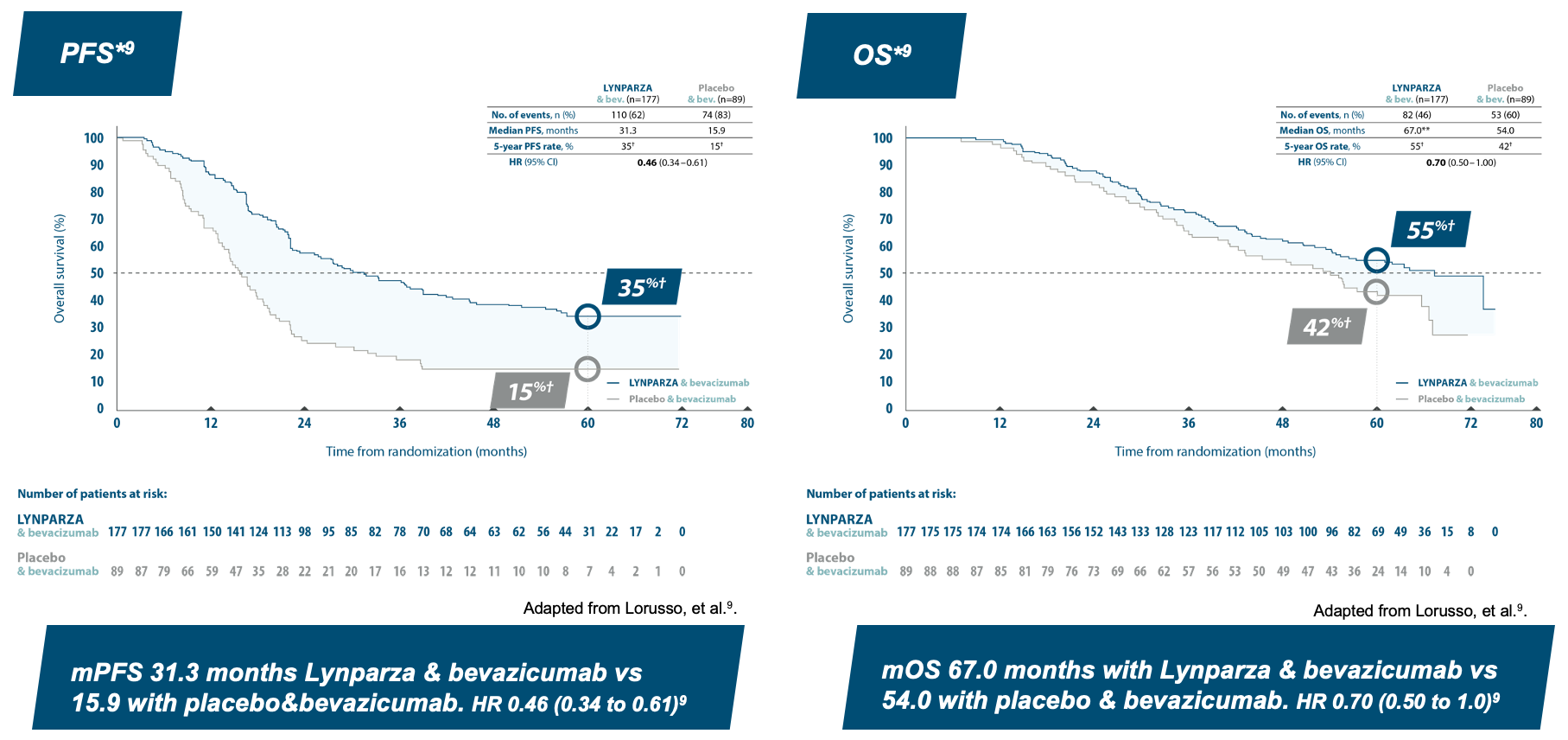
*Higher risk defined as: FIGO Stage III patients with upfront surgery and residual disease or NACT, FIGO Stage IV patients. **Unstable median due to lack of events. †Kaplan-Meier estimates.
LYNPARZA & bevacizumab improves both PFS and OS9
Almost 9 of 10 patients still alive at 5 years in ”lower risk” group9
5 year pre-specified exploratory subgroup analysis: HRD-positive patients ”lower risk*”
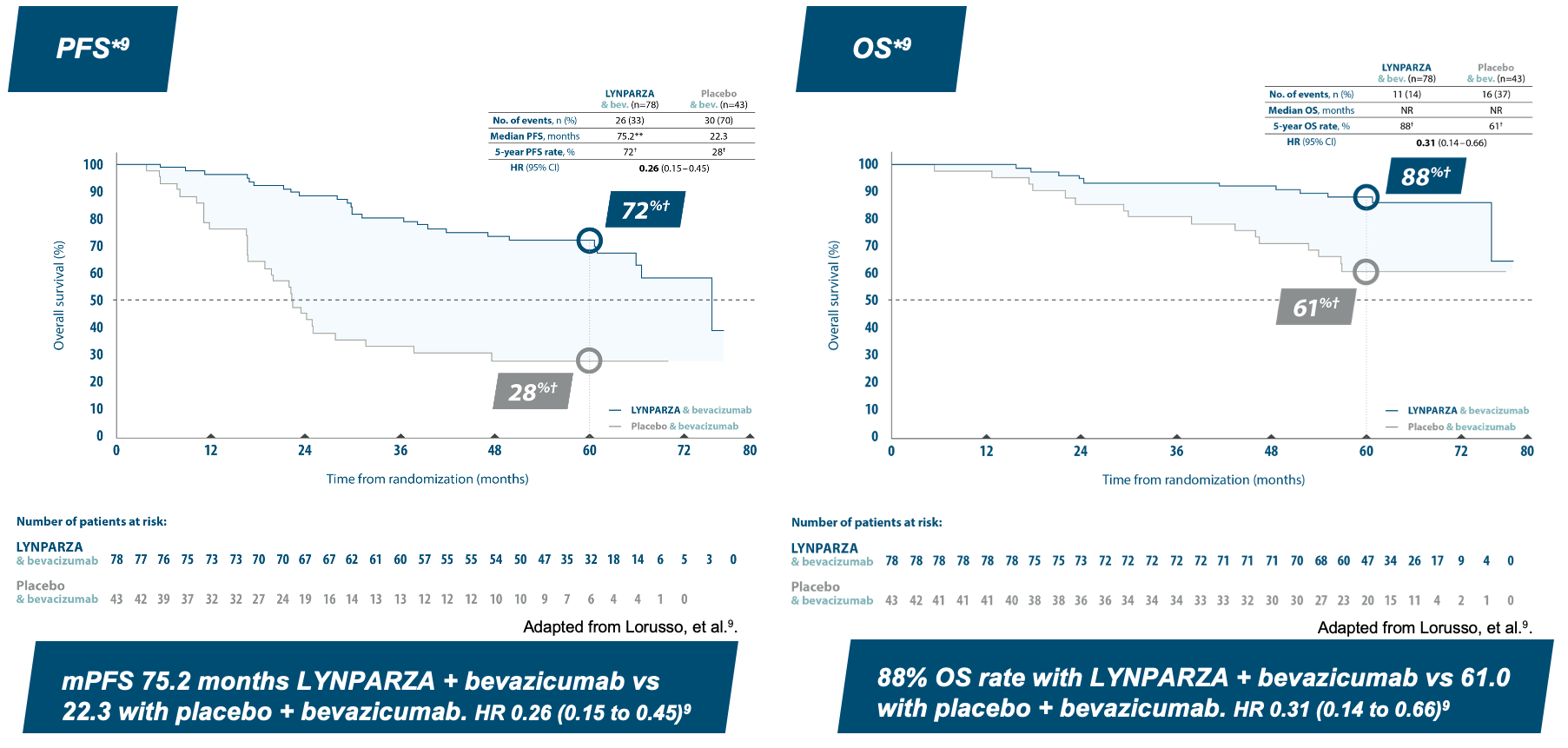
*Lower risk defined as FIGO Stage III patients with upfront surgery and complete resection. **Unstable median due to lack of events. †Kaplan-Meier estimates.
Consider PAOLA-1 regimen to all eligible HRD-positive patients for opportunity for long-term PFS and OS1,2
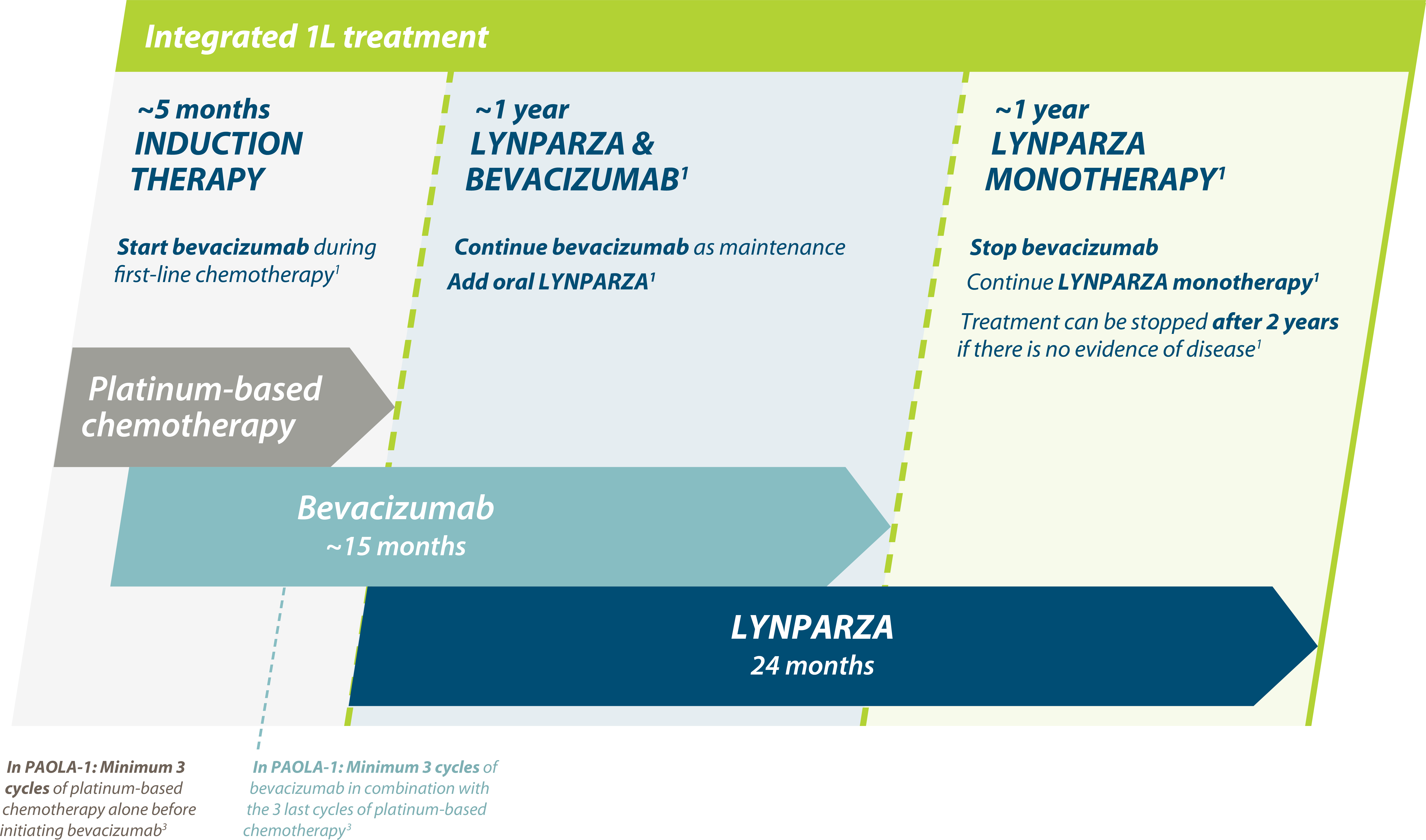
Adapted from Ray-Coquard, et al. 2019.2
Safety profile
Adverse events in PAOLA-1 were generally consistent with the known safety profiles of LYNPARZA and bevacizumab individually.
After 5-year-follow-up no new safety signals were observed and MDS/AML/AA, pneumonitis and new primary malignancy incidence remained low. The most common AEs of any grade were fatigue/nausea, hypertension, anemia and lymphopenia. And the most common grade ≥ 3 AE was anemia.
AEs were predominantly grade 1-2 and led to dose reduction in 41% with LYNPARZA+bevacizumab vs 7% with bevacizumab alone.2,5
Full safety information available in Lynparza SPC.
Lynparza in 1L advanced ovarian cancer
Below you can find information about Lynparza treatment and diagnostics in 1L advanced ovarian cancer.
Lynparza (olaparib) - viktig informasjon (utvalg)
Indikasjoner:
Ovarialkreft: Monoterapi til vedlikeholdsbehandling av voksne med avansert (FIGO trinn III og IV) BRCA1/2-mutert (kimbanen og/eller somatisk) høygradig kreft i ovarieepitel, eggleder eller primær peritonealkreft, som responderer (fullstendig eller delvis) etter avsluttet førstelinje platinabasert kjemoterapi. Monoterapi til vedlikeholdsbehandling av voksne med tilbakefall av platinasensitiv høygradig kreft i ovarieepitel eller eggleder, eller primær peritonealkreft, som responderer (fullstendig eller delvis) på platinabasert kjemoterapi. I kombinasjon med bevacizumab til vedlikeholdsbehandling av voksne med avansert (FIGO trinn III og IV) høygradig kreft i ovarieepitel, eggleder eller primær peritonealkreft, som responderer (fullstendig eller delvis) etter avsluttet førstelinje platinabasert kjemoterapi i kombinasjon med bevacizumab, og hvor kreften er forbundet med defekt homolog rekombinasjon (HRD)-positiv status, definert av enten en BRCA1/2-mutasjon og/eller genomisk ustabilitet.
Dosering: Behandling med Lynparza bør initieres og overvåkes av lege med erfaring i bruk av legemidler til kreftbehandling. Genomisk testing er nødvendig før oppstart ved flere av Lynparzas indikasjoner, se pkt. 4.2 i SPC. Anbefalt dose av olaparib, enten som monoterapi eller i kombinasjon med andre legemidler: 300 mg (2 tabletter à 150 mg) 2 ganger daglig (tilsv. daglig totaldose på 600 mg). Tabletter med styrken 100 mg er tilgjengelig for dosereduksjon ved bivirkninger, ved samtidig bruk av sterk/moderat CYP3A-hemmer eller ved moderat nedsatt nyrefunksjon. For dosering av legemiddel i kombinasjon med Lynparza og behandlingens varighet, se pkt. 4.2. i SPC.
Kontraindikasjoner: Amming under behandling og i 1 måned etter siste dose.
Forsiktighetsregler: Blodtelling før behandlingsoppstart og deretter månedlig, er anbefalt de første 12 månedene av behandlingen og periodevis etter dette. Behandlingen skal avbrytes og hensiktsmessig hematologisk testing igangsettes, ved alvorlig hematologisk toksisitet eller behov for blodtransfusjon. Forblir blodparametrene klinisk unormale etter 4 ukers behandlingsavbrudd, anbefales benmargsanalyse og/eller cytogenetisk blodanalyse. MDS/AML: Rapportert hos et lite antall ved monoterapi eller i kombinasjon med annen kreftbehandling. Dersom MDS og/eller AML blir diagnostisert, anbefales det at pasienten får egnet behandling mot disse sykdommene. Olaparib bør seponeres, og ikke gis i kombinasjon med annen kreftbehandling. Pneumonitt: Ved bekreftet pneumonitt avbrytes behandlingen, og pasienten behandles hensiktsmessig. Behandlingen bør avbrytes og utredes raskt, ved nye eller forverrede respiratoriske symptomer som dyspné, hoste og feber, eller radiologisk abnormitet. Bilkjøring og betjening av maskiner: Asteni, tretthet og svimmelhet er rapportert, og pasienter som opplever disse symptomene bør utvise forsiktighet ved bilkjøring eller ved bruk av maskiner. Viktige interaksjoner: Samtidig bruk av sterke eller moderate CYP3A-induktorer eller CYP3A hemmere er ikke anbefalt. Graviditet: Kan gi fosterskade og skal derfor ikke brukes under graviditet.
Hyppigste bivirkninger ved monoterapi: Kvalme, oppkast, diaré, dyspepsi, fatigue/asteni, hodepine, dysgeusi, nedsatt appetitt, svimmelhet, hoste, dyspné, anemi, nøytropeni, og leukocytopeni.
Pakninger og priser: Tablett 100 mg, 150 mg: 56 blisterpakning: kr: 27 754,60
AstraZeneca AS - www.astrazeneca.no – P. box 6050 Etterstad - 0601 Oslo
For fullstendig informasjon, les mer på www.felleskatalogen.no
ID: NO-13966-04-25-ONC
References:
-
Lynparza SPC
-
Ray-Coquard I, et al. N Engl J Med. 2019;381:2416–28.
-
Gambara G, Gaebler M, Keiholz U, et al. From Chemotherapy to Combined Targeted Therapeutics: In Vitro and vivo Models to Decipher Intra-tumor Heterogenety. Front Pharmacol. 2028 Feb 14;9:77. Doi: 10.3389/fphar.2018.00077.
-
Saux OL, Vanacker H, Guermazi F, et al. Poly (ADP-ribose) polymerase inhibitors in combination with anti-angiogenic cancer. Future Oncol. 2021. Mar 17. Doi:10.2217/fon-2021-0059
-
Ray-Coquard I, et al. Ann Oncol. 2023;34(8):681-92).
-
Giornelli GH et al. Management of relapsed ovarian cancer: A review. SpringerPlus. 2016;5:1197.
-
du Bois A, et al. Role of surgical outcome as prognostic factor in advanced epithelial ovarian cancer: a combined exploratory analysis of 3 prospectively randomized phase 3 multicenter trials.Cancer.
-
Lorusso D, et al. Int J Gynecol Cancer. 2024;34:550-8
-
Lorusso D, et al. Int J Gynecol Cancer 2023;0:1–9. doi:10.1136/ijgc-2023-004995



