Lynparza (olaparib) - viktig informasjon (utvalg)
Indikasjoner:
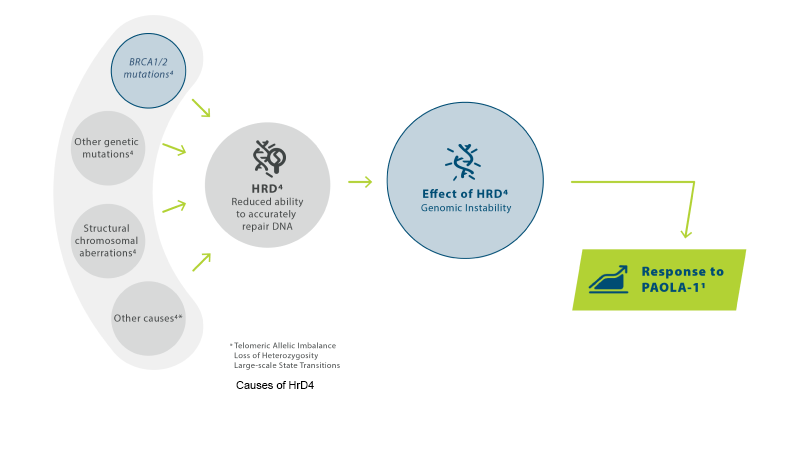
Ovarialkreft: Monoterapi til vedlikeholdsbehandling av voksne med avansert (FIGO trinn III og IV) BRCA1/2-mutert (kimbanen og/eller somatisk) høygradig kreft i ovarieepitel, eggleder eller primær peritonealkreft, som responderer (fullstendig eller delvis) etter avsluttet førstelinje platinabasert kjemoterapi. Monoterapi til vedlikeholdsbehandling av voksne med tilbakefall av platinasensitiv høygradig kreft i ovarieepitel eller eggleder, eller primær peritonealkreft, som responderer (fullstendig eller delvis) på platinabasert kjemoterapi. I kombinasjon med bevacizumab til vedlikeholdsbehandling av voksne med avansert (FIGO trinn III og IV) høygradig kreft i ovarieepitel, eggleder eller primær peritonealkreft, som responderer (fullstendig eller delvis) etter avsluttet førstelinje platinabasert kjemoterapi i kombinasjon med bevacizumab, og hvor kreften er forbundet med defekt homolog rekombinasjon (HRD)-positiv status, definert av enten en BRCA1/2-mutasjon og/eller genomisk ustabilitet.
Dosering: Behandling med Lynparza bør initieres og overvåkes av lege med erfaring i bruk av legemidler til kreftbehandling. Genomisk testing er nødvendig før oppstart ved flere av Lynparzas indikasjoner, se pkt. 4.2 i SPC. Anbefalt dose av olaparib, enten som monoterapi eller i kombinasjon med andre legemidler: 300 mg (2 tabletter à 150 mg) 2 ganger daglig (tilsv. daglig totaldose på 600 mg). Tabletter med styrken 100 mg er tilgjengelig for dosereduksjon ved bivirkninger, ved samtidig bruk av sterk/moderat CYP3A-hemmer eller ved moderat nedsatt nyrefunksjon. For dosering av legemiddel i kombinasjon med Lynparza og behandlingens varighet, se pkt. 4.2. i SPC.
Kontraindikasjoner: Amming under behandling og i 1 måned etter siste dose.
Forsiktighetsregler: Blodtelling før behandlingsoppstart og deretter månedlig, er anbefalt de første 12 månedene av behandlingen og periodevis etter dette. Behandlingen skal avbrytes og hensiktsmessig hematologisk testing igangsettes, ved alvorlig hematologisk toksisitet eller behov for blodtransfusjon. Forblir blodparametrene klinisk unormale etter 4 ukers behandlingsavbrudd, anbefales benmargsanalyse og/eller cytogenetisk blodanalyse. MDS/AML: Rapportert hos et lite antall ved monoterapi eller i kombinasjon med annen kreftbehandling. Dersom MDS og/eller AML blir diagnostisert, anbefales det at pasienten får egnet behandling mot disse sykdommene. Olaparib bør seponeres, og ikke gis i kombinasjon med annen kreftbehandling. Pneumonitt: Ved bekreftet pneumonitt avbrytes behandlingen, og pasienten behandles hensiktsmessig. Behandlingen bør avbrytes og utredes raskt, ved nye eller forverrede respiratoriske symptomer som dyspné, hoste og feber, eller radiologisk abnormitet. Bilkjøring og betjening av maskiner: Asteni, tretthet og svimmelhet er rapportert, og pasienter som opplever disse symptomene bør utvise forsiktighet ved bilkjøring eller ved bruk av maskiner. Viktige interaksjoner: Samtidig bruk av sterke eller moderate CYP3A-induktorer eller CYP3A hemmere er ikke anbefalt. Graviditet: Kan gi fosterskade og skal derfor ikke brukes under graviditet.
Hyppigste bivirkninger ved monoterapi: Kvalme, oppkast, diaré, dyspepsi, fatigue/asteni, hodepine, dysgeusi, nedsatt appetitt, svimmelhet, hoste, dyspné, anemi, nøytropeni, og leukocytopeni.
Pakninger og priser: Tablett 100 mg, 150 mg: 56 blisterpakning: kr: 27 754,60
AstraZeneca AS - www.astrazeneca.no – P. box 6050 Etterstad - 0601 Oslo
For fullstendig informasjon, les mer på www.felleskatalogen.no
ID: NO-13966-04-25-ONC