Hold deg oppdatert!
Få relevant informasjon om blant annet:
- Medisinske nyheter
- Webinarer
- Pasientstøtte
- Produktinformasjon
- Bivirkningsrapportering
Du kan når som helst trekke tilbake ditt samtykke.

PROfound is a prospective, multicentre, randomised, open-label, Phase III trial testing the efficacy and safety of Lynparza (olaparib) versus enzalutamide or abiraterone in patients with metastatic castration-resistant prostate cancer (mCRPC) who have progressed on prior treatment with novel hormonal agents (NHAs) (abiraterone or enzalutamide) and have a qualifying tumour mutation in BRCA1/2, ATM or one of 12 other genes involved in the homologous recombination repair (HRR) pathway.2
The trial was designed to analyse patients with HRR gene mutations in two cohorts: the primary endpoint was rPFS in those with mutations in BRCA1/2 or ATM genes and then, if Lynparza showed clinical benefit, a formal analysis was performed of the overall trial population of patients with HRR gene mutations (BRCA1/2, ATM, CDK12 and 11 other HRR gene mutations).2
Lynparza (olaparib) is the first PARP inhibitor approved in the EU in biomarker-selected advanced prostate cancer. Lynparza (olaparib) was approved by EU for patients with mCRPC with breast cancer susceptibility gene 1/2 (BRCA1/2) mutations, a subpopulation of HRR gene mutations in november 2020.1
The approval by the European Commission was based on a subgroup analysis of the PROfound Phase III trial which showed Lynparza (olaparib) demonstrated a substantial improvement in rPFS and overall survival (OS) versus enzalutamide or abiraterone in men with BRCA1/2 mutations.1,2
The subgroup analysis of mCRPC patients with BRCA1/2 mutations from the PROfound Phase III trial demonstrated that:
For disease progression based on rPFS (primary endpoint):
For patient survival based on OS (secondary endpoint):
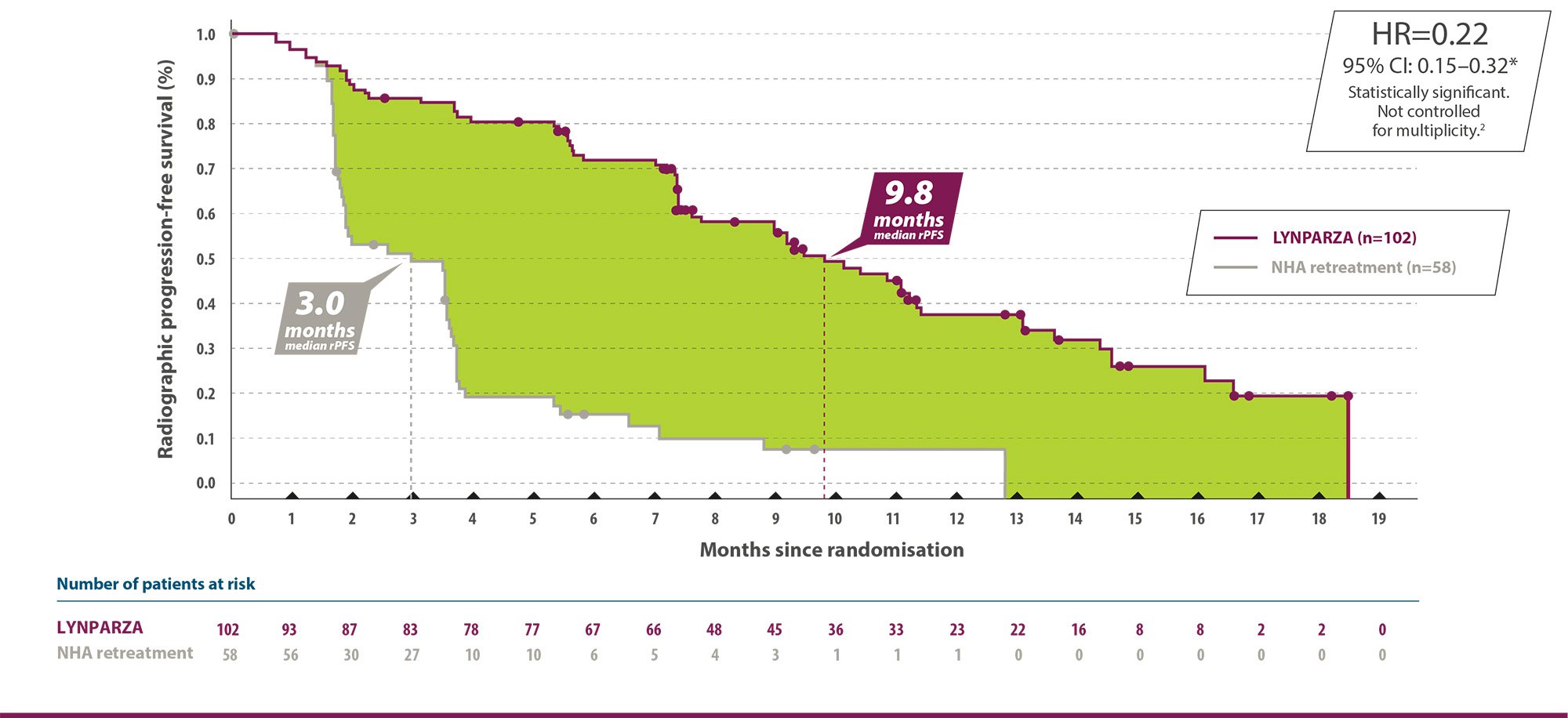
*The HR and CI were calculated using a Cox proportional hazards model that contains terms for treatment, factor and treatment by factor interaction.1 Adapted from LYNPARZA Summary of Product Characteristics.
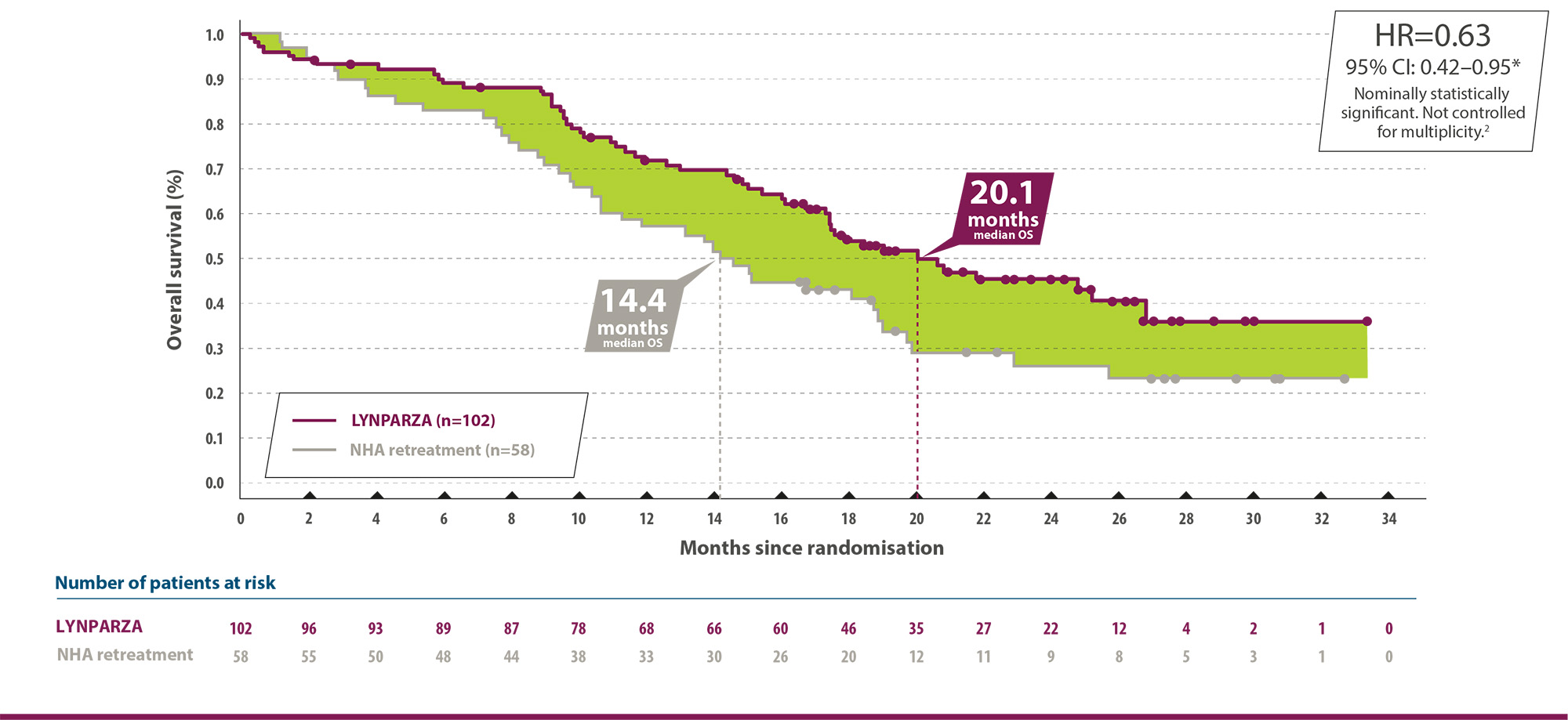
69% of the patients in the control arm in cohort A received Lynparza which could have lowered the difference in overall survival.3
*The HR and CI were calculated using a Cox proportional hazards model that contains terms for treatment, factor and treatment by factor interaction.1 Adapted from LYNPARZA Summary of Product Characteristics.
Haematological toxicity
Baseline testing, followed by monthly monitoring, of complete blood counts is recommended for the first 12 months of treatment and periodically after this time to monitor for clinically significant changes in any parameter during treatment (see section 4.8).
Myelodysplastic syndrome/Acute myeloid leukaemia
If MDS/AML is confirmed, Lynparza should be discontinued and the patient treated appropriately.
Venous Thromboembolic Events
Monitor patients for clinical signs and symptoms of venous thrombosis and pulmonary embolism and treat as medically appropriate.
Pneumonitis
If patients present with new or worsening respiratory symptoms such as dyspnoea, cough and fever, or an abnormal chest radiologic finding is observed, Lynparza treatment should be interrupted and prompt investigation initiated.
Hepatotoxicity
If clinical symptoms or signs suggestive of hepatotoxicity develop, prompt clinical evaluation of the patient and measurement of liver function tests should be performed. In case of suspected drug-induced liver injury (DILI), treatment should be interrupted.
The most common side effects in the PROfound trial (greater than or equal to 20 % of patients) were anemia (46%), nausea (41%), fatigue or asthenia (41%), decreased apetite (30%) and diarrhea (21%). Grade 3 or higher adverse events were anemia (21%), fatigue or asthenia (3%), vomiting (2%), urinary tract infection (2%), dyspnea (2%), nausea (1%), decreased apetite (1%), back pain (<1%), diarrhea (<1%) and arthralgia (<1%).2
**safety data is from patients in cohort cohort A+B in the study (N=256), not only from the sub population with BRCA (refer to section PROFOUND study design and patient characteristics).
The primary results and overall survival results from the PROfound Phase III trial was published in The New England Journal of Medicine in 2020.1,4
In this study:
Demographic and baseline characteristics were generally well balanced between olaparib and the comparator treatment arms in patients with BRCA1/2 mutations. The median age was 68 years and 67 years in the olaparib and comparator treatment arms, respectively. Previously treatment in the olaparib arm was 71% taxane, 41% enzalutamide, 37% abiraterone acetate and 20% both enzalutamide and abiraterone acetate. Prior treatment in the comparator arm was 60% taxane, 50% enzalutamide, 36% abiraterone acetate and 14% both enzalutamide and abiraterone acetate. Fifty-eight percent (58%) of patients in the olaparib arm and 55% in the comparator arm had measurable disease at the start of the study. The proportion of patients with metastases in the skeleton, lymph nodes, airways and liver were 89%, 62%, 23% and 12%, respectively in the olaparib arm and 86%, 71%, 16% and 17% respectively in the comparator arm. The majority of the patients in both treatment arms had an ECOG of 0 or 1 (93%). Baseline pain score (BPI-SF worst pain) was 0 - < 2 (52%), 2 - 3 (10%) or > 3 (34%) in the olaparib arm and 0 - < 2 (45%), 2 - 3 (7%) or > 3 (45%) in the comparator arm. Median baseline-PSA was 57.48 microg/l in the olaparib arm and 103.95 microg/l in the comparator arm.The primary endpoint of the study was radiological progression-free survival (rPFS) in the cohort A determined by BICR using RECIST 1.1 (soft tissue) and the "Prostate Cancer Working Group” (PCWG3) (skeleton). Key secondary endpoints included confirmed objectiveresponse rate (ORR) at BICR, rPFS at BICR, time to pain progression (TTPP) and overall survival (OS).1,2
LYNPARZA®(olaparib) er en potent hemmer av humane poly (ADP-ribose) polymerase (PARP-1, PARP-2 og PARP-3)-enzymer. Hemmer veksten av selekterte tumorcellelinjer in vitro og tumorvekst in vivo, enten som eneste behandling eller i kombinasjon med etablerte kjemoterapier.
Prostatakreft: Som monoterapi til behandling av voksne med metastatisk kastrasjonsresistent prostatakreft (mCRPC) og BRCA1/2 mutasjoner (kimbane og/eller somatiske) som har progrediert etter tidligere behandling som inkluderte et nytt hormonlegemiddel. I kombinasjon med abirateron og prednison eller prednisolon til behandling av voksne pasienter med mCRPC, der kjemoterapi ikke er klinisk indisert (se pkt 5.1 i SPC).
DOSERING OG ADMINISTRASJONSMÅTE
Behandling med Lynparza bør initieres og overvåkes av lege med erfaring i bruk av legemidler til kreftbehandling.
Dosering: Lynparza er tilgjengelig som tabletter à 100 mg og 150 mg. Anbefalt dose av Lynparza som monoterapi eller i kombinasjon med med abirateron og prednison eller prednisolon for prostatakreft eller med endokrin behandling er 300 mg (to tabletter à 150 mg) som skal tas to ganger daglig, tilsvarende en daglig dose på totalt 600 mg. Tablett à 100 mg er tilgjengelig for dosereduksjon. Hvis teksten/saken omhandler kombinasjonsbehandling så skal det legges til doseringsinformasjon om det aktuelle kombinasjonspreparatet:
Lynparza i kombinasjon med endokrin behandling: Behandling med gonadotropinfrigjørende hormon (GnRH)-analog skal fortsettes under behandling av alle pasienter, eller pasientene skal ha gjennomgått bilateral orkiektomi før behandlingen. Se den fullstendige produktinformasjonen for legemidler som brukes til endokrin behandling i kombinasjon med Lynparza (GnRH-analog), for informasjon om anbefalt dosering. Ved bruk av Lynparza i kombinasjon med abirateron til behandling av pasienter med mCRPC er
abiraterondosen 1000 mg peroralt én gang daglig (se pkt. 5.1 i SPC). Abirateron skal gis sammen med prednison eller prednisolon 5 mg peroralt to ganger daglig. Behandling med gonadotropinfrigjørende hormon (GnRH)-analog skal fortsettes under behandling av alle pasienter, eller pasientene skal ha gjennomgått bilateral orkiektomi før behandlingen. Se preparatomtalen for abirateron.
UTVALGT SIKKERHETSINFORMASJON
FORSIKTIGHET UTVISES VED: Hematologisk toksisitet: Blodtelling før behandlingsoppstart og deretter månedlig, er anbefalt de første 12 månedene av behandlingen og periodevis etter dette tidspunktet for å overvåke klinisk signifikante endringer av verdiene under behandling. Myelodysplastisk syndrom/akutt myelogen leukemi: Dersom MDS og/eller AML blir diagnostisert under behandling med Lynparza, skal Lynparza seponeres og pasienten skal få hensiktsmessig behandling. Venøse tromboemboliske hendelser: Pasientene skal overvåkes med tanke på kliniske tegn og symptomer på venetrombose og lungemboli og behandles på medisinsk hensiktsmessig måte. Pneumonitt: Hvis pasienten får nye, eller en forverring av respiratoriske symptomer som dyspné, hoste og feber, eller et unormalt radiologisk funn observeres i brystet, bør behandling med Lynparza avbrytes og utredning igangsettes raskt. Levertoksisitet: Dersom det utvikles kliniske symptomer eller tegn som tyder på levertoksisitet, må klinisk vurdering av pasienten og måling av leverfunksjonsprøver utføres raskt. Dersom det mistenkes legemiddelutløst leverskade (DILI), skal behandlingen avbrytes. Fertilitet, graviditet: Mannlige pasienter må bruke kondom og deres fertile kvinnelige partnere skal bruke sikker prevensjon under behandling og i 3 måneder etter å ha fått siste dose av Lynparza (se pkt. 4.6 i SPC). Se pkt. 4.4 i SPC for mer informasjon om advarsler og forsiktighetsregler.
VIKTIGE INTERAKSJONER: Samtidig administrering av Lynparza med kraftige eller moderate CYP3A-hemmere eller CYP3A-induktorer anbefales ikke. Se pkt. 4.2 og 4.5 i SPC for mer informasjon dersom en kraftig eller moderat CYP3A-hemmer eller CYP3A-induktor likevel må administreres samtidig med Lynparza. Se pkt 4.5 i SPC for mer informasjon om andre former for interaksjoner.
VIKTIGE BIVIRKNINGER: De hyppigste observerte bivirkningene på tvers av kliniske studier hos pasienter som fikk Lynparza som monoterapi (≥ 10 %) var kvalme, oppkast, diaré, dyspepsi, fatigue/asteni, hodepine, dysgeusi, nedsatt appetitt, svimmelhet, hoste, dyspné, anemi, nøytropeni, , og leukocytopeni. Bivirkninger førte til doseavbrudd og/eller dosereduksjon hos 50,7% av pasientene ved bruk i kombinasjon med abirateron. Bivirkningene som oftest førte til doseavbrudd og/eller dosereduksjon, var anemi (17,1%), fatigue/asteni (5,5%), kvalme (4,1%) og nøytropeni (3,4%).
Pakninger og priser: Tabletter: 100 mg: 56 stk. kr 30 297,70. 150 mg: 56 stk. kr 31 636,10.
Reseptgruppe C. Refusjon: H-resept.
Refusjonsberettiget bruk: Der det er utarbeidet nasjonale handlingsprogrammer/nasjonal faglig retningslinje og/eller anbefalinger fra RHF/LIS spesialistgruppe skal rekvirering gjøres i tråd med disse. De regionale helseforetakenes anbefalinger: Onkologi og kolonistimulerende legemidler Vilkår: (216) Refusjon ytes kun etter resept fra sykehuslege eller avtalespesialist.
Beslutning i Beslutningsforum for nye metoder (19.06.2023): Olaparib (Lynparza) innføres som monoterapi til behandling av voksne pasienter med metastatisk kastrasjonsresistent prostatakreft og BRCA1/2-mutasjoner (kimbane og/eller somatiske) som har progrediert etter behandling med nye hormonelle legemidler og hvor behandling med docetaksel, kabazitaksel og radium-223 har gitt utilstrekkelig effekt eller ikke er egnet.
Beslutning i Beslutningsforum for nye metoder (22.01.2024): Olaparib (Lynparza) og abirateron i kombinasjon med prednison eller prednisolon innføres til behandling av voksne pasienter med metastatisk kastrasjonsresistent prostatakreft (mCRPC), der kjemoterapi ikke er klinisk indisert.
Markedsføringsinnehaver: AstraZeneca AS, Karvesvingen 7, 0579 Oslo, tel. 21006400
Før forskrivning av LYNPARZA, se FK-tekst eller SPC på www.felleskatalogen.no
NO-13051-10-24-ONC

Lynparza in combination with abiraterone for patients with metastatic prostate cancer
Learn more
Vil du vite mer om Lynparzas indikasjoner og bruken i kliniske studier? Vi har oppsummert relevant informasjon for deg, sammen med grafer og pedagogiske videoer.
Learn moreProduktresume for Lynparza (olaparib), https://www.felleskatalogen.no
de Bono J, Mateo J, Fizazi K, et al. Olaparib for metastatic castration-resistant prostate cancer. N Engl J Med. 2020;382(22):2091–2102.
Evans E, Hawkins N, Dequen-O' Bryne P, et al. Exploring the Impact of Treatment Switching on Overall Survival from the PROfound Study in Homologous Recombination Repair (HRR)-Mutated Metastatic Castration-Resistant Prostate Cancer (mCRPC). Target Oncology. 2021;16(5):613-623.
Hussain M, Mateo J, Fizazi K, et al. Survival with olaparib in metastatic castration-resistant prostate cancer. N Engl J Med. 2020;383:2345–2357.
de Bono J, Fizazi K, Saad F, et al. Central, prospective detection of homologous recombination repair gene mutations (HRRm) in tumour tissue from >4000 men with metastatic castration-resistant prostate cancer (mCRPC) screened for the PROfound study. Ann Oncol. 2019;30(5):V328-V329.
Castro E, Goh E, Olmos D, et al. Germline BRCA mutations are associated with higher risk of nodal involvement, distant metastasis, and poor survival outcomes in prostate cancer. J Clin Oncol. 2013;31(14):1748–1757.
Castro E, Goh E, Leongamornlet D, et al. Effect of BRCA mutations on metastatic relapse and cause-specific survival after radical treatment for localised prostate cancer. Eur Urol. 2015; 68(2):186–193.
Na R, Zheng SL, Han M, et al. Germline mutations in ATM and BRCA1/2 distinguish risk for lethal and indolent prostate cancer and are associated with early age at death. Eur Urol. 2017; 71(5):740–747.
Kirby M, Hirst C, Crawford ED. Characterising the castration-resistant prostate cancer population: a systematic review. Int J Clin Pract. 2011;65(11):1180-1192.
Wu J, Lu L, Yu X. The role of BRCA1 in DNA damage response. Protein Cell. 2010;1(2):117-123.
Roy R, Chun J, Powell SN. BRCA1 and BRCA2: different roles in a common pathway of genome protection. Nat Rev Cancer. 2011;12(1):68-78.
Gorodetska I, Kozeretska I, Dubrovska A. BRCA Genes: The Role in Genome Stability, Cancer Stemness and Therapy Resistance. J Cancer. 2019;10(9):2109-2127.
Cheng HH, Sokolova AO, Schaeffer EM, et al. Germline and somatic mutations in prostate cancer for the clinician. J Natl Compr Canc Netw. 2019;17(5):515–521.
Abida W, Armenia J, Gopalan A, et al. Prospective genomic profiling of prostate cancer across disease states reveals germline and somatic alterations that may affect clinical decision making. JCO Precis Oncol. 2017.
AstraZeneca og MSD er i en allianse
for å promotere Lynparza