Hold deg oppdatert!
Få relevant informasjon om blant annet:
- Medisinske nyheter
- Webinarer
- Pasientstøtte
- Produktinformasjon
- Bivirkningsrapportering
Du kan når som helst trekke tilbake ditt samtykke.
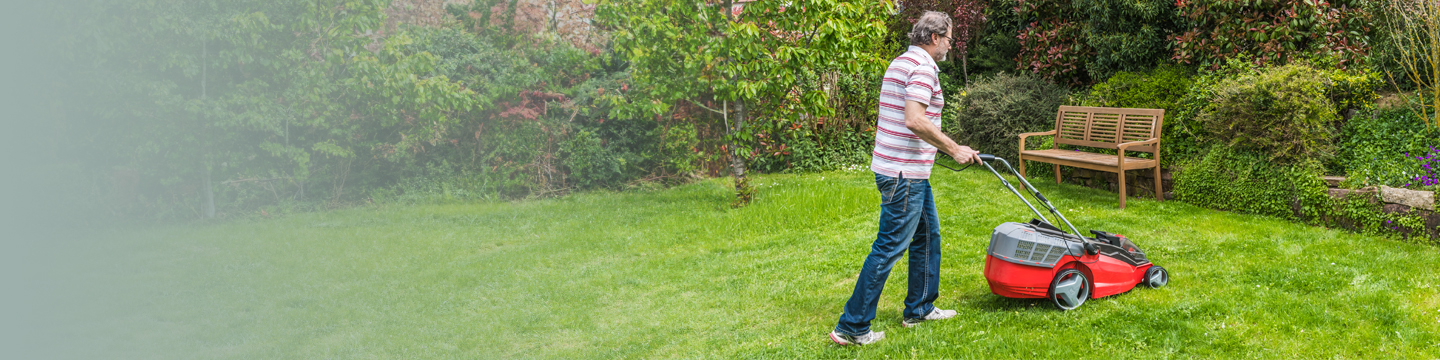
Fasenra (benralizumab)
Hvilke pasienter kan være aktuelle for Fasenra?
Behandlingsmålet ved alvorlig astma er likt som hos andre personer med astma: Normal lungefunksjon, god astmakontroll (inkludert fravær av nattlige oppvåkninger med hoste og tett bryst) og maksimalt to episoder pr. uke med astmasymptomer og/eller behov for hurtigvirkende bronkodilatator.1
Eosinofiler kan gjøre at inflammasjonen sprer seg, og lede til flere forverringer, økt slimproduksjon og skader på luftveiene.3 For pasienter med alvorlig eosinofil astma kan eosinofildrevet inflammasjon føre til:

Økte nivåer av eosinofiler hos pasienter med alvorlig ukontrollert astma kan bidra til 2 ganger høyere risko for å oppleve ≥2 forverringer på 1 år.6,*

Pasienter med alvorlig ukontrollert astma har nesten 3 ganger høyere risiko for å oppleve minst 1 sykehusinnleggelse i året, sammenliknet med pasienter som ikke har alvorlig ukontrollert astma.7,†,‡
Pasienter med alvorlig ukontrollert astma har nesten 3 ganger så høy risiko for å måtte trenge ≥5 mg orale kortikosteroider daglig, sammenliknet med pasienter som ikke har alvorlig ukontrollert astma.8,†,§

Eksempel på eosinofil pasient (ikke reell pasient)**:
Jeg elsker å undervise på barneskolen og ønsker ikke å pensjonere meg. Men det er så vanskelig å håndtere min alvorlige astma at jeg sliter med å holde følge med elevene mine.
Mary (47), lærer

Eksempel på pasient (ikke reell pasient)*** med alvorlig eosinofil astma som regelmessig bruker orale kortikosteroider (OCS):
Jeg er bekymret for vektøkningen og bivirkningene ved orale kortikosteroider, men det er det eneste som hjelper meg akkurat nå. Jeg trenger noe annet.
Mark (49), salgsleder
Fasenra er indisert som tillegg til vedlikeholdsbehandling hos voksne med alvorlig eosinofil astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider samt langtidsvirkende betaagonister.
Feber, reaksjon på injeksjonsstedet, overfølsomhetsreaksjon, faryngitt, hodepine. Skal ikke brukes til å behandle akutte astmaeksaserbasjoner.
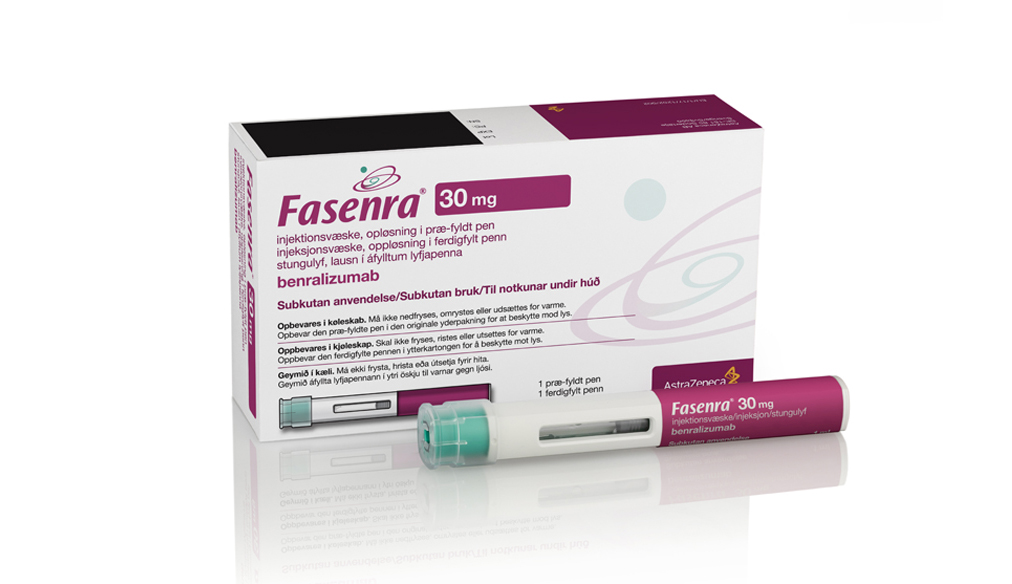
Fasenra doseres hver 8. uke, etter oppstartsperiode. Kan settes av pasienten selv eller helsepersonell13...
Se praktisk informasjon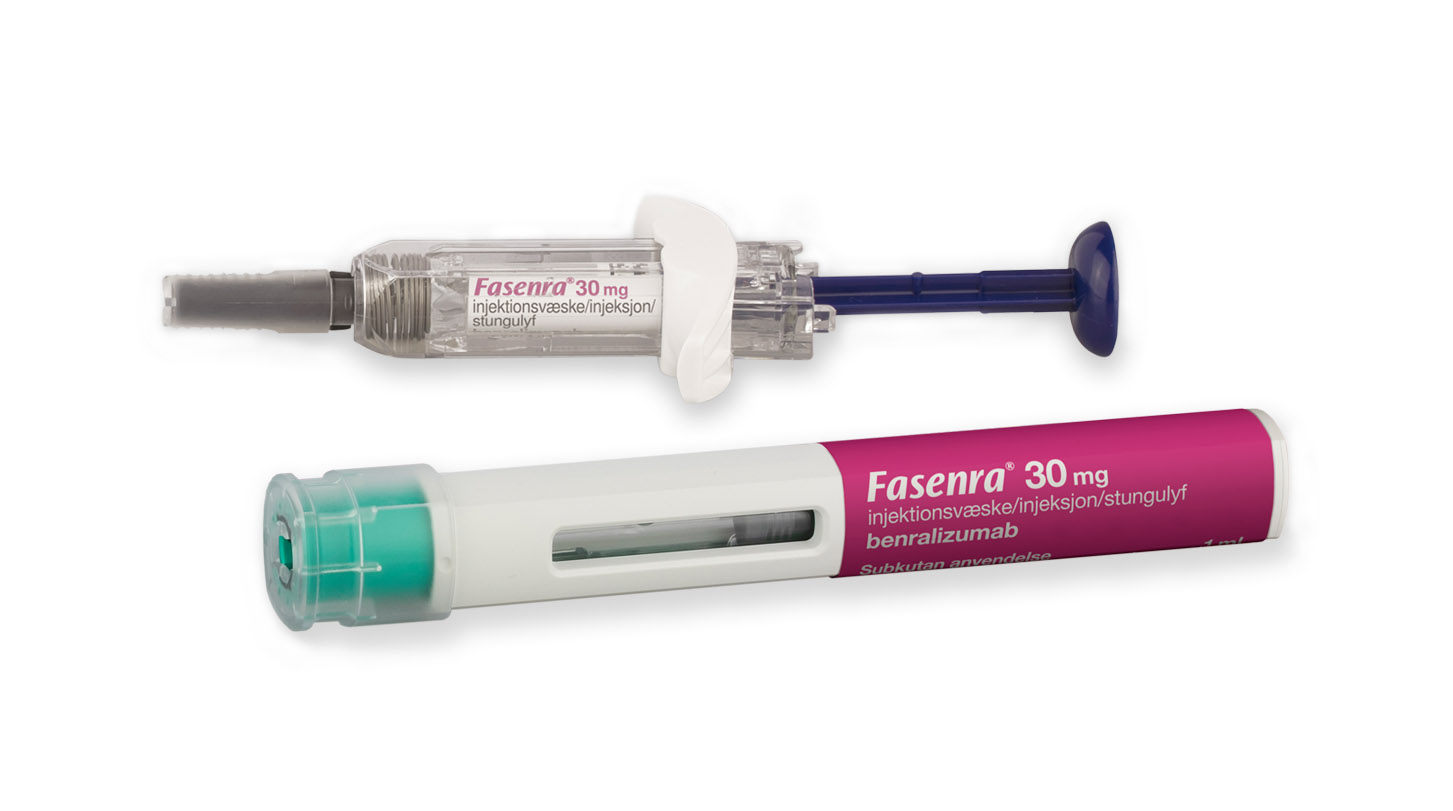
Ta kontakt med Beate Furuseth eller Arne Helvig for demonstrasjonsmateriell. Vi tar kontakt for møte.
Kontakt
Kommentarer og opplysninger til pasientprofiler
* En observasjonsstudie som evaluerte sammenhengene mellom EOS-nivåer og astmaforverringer i pasienter med alvorlig ukontrollert astma (n=261). Astmaforverringer er definert som en sykehusinnleggelse eller besøk på akuttmottak/legevakt hvor astma er den primære diagnosen, eller forskrivning av OCS innen ± 7 dager etter legebesøk som følge av ukontrollert astma (dvs. akutt eksaserbasjon, status asthmaticus, akutt astmaanfall, ukontrollert astma eller asthmatic bronchitis). Poisson-regresjonsmodell ble brukt for å estimere risikoforholdet for bEOS-nivåer ≥400 celler/μl (n=77) versus <400 celler/μl (n=184) for ≥2 astmaeksaserbasjoner (1,55; 95 % CI, 1,02-2,35; P=0,04).6
† En observasjonsstudie som sammenligner pasienter med alvorlig ukontrollert astma (n=585) med pasienter uten alvorlig ukontrollert astma (n=25,350). Alvorlig ukontrollert astma ble definert som ≥2 eksaserbasjoner, ≥6 dispenserte beholdere med middels eller høydose ICS alene eller med en LABA og ≥3 dispenserte ikke-ICS-kontroller i året før registrering. Poisson-regresjonsmodeller ble brukt som statistisk metode.7
‡ Estimert risikoforhold for pasienter med alvorlig ukontrollert astma (n=22) og pasienter uten alvorlig ukontrollert astma (n=210) med ≥1 astma-sykehusinleggelse (2,92; 95 % CI, 1,83-4,67; P<0,001).7
§ Estimert risikoforhold for pasienter med alvorlig ukontrollert astma (n=65) og pasienter uten alvorlig ukontrollert astma (n=414) behandlet med ≥5 mg/dag av orale kortikosteroider (2,80; 95 % CI, 2,12-3,69; P<0,001).7
** Pasienten er representativ for populasjonen i SIROCCO med EOS ≥300 celler/μl i blod og 2 eller flere forverringer foregående år.10
*** Pasienten er representativ for populasjonen i i ZONDA med EOS ≥150 celler/μl i blod og minst 1 forverring i foregående år og kronisk bruk av orale kortikosteroider.11
Indikasjon: Astma: Fasenra er indisert som tillegg til vedlikeholdsbehandling hos voksne med alvorlig eosinofil astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider samt langtidsvirkende beta-agonister.
Eosinofil granulomatose med polyangiitt (EGPA): Fasenra er indisert som tilleggsbehandling hos voksne pasienter med relapserende eller refraktær eosinofil granulomatose med polyangiitt.
Dosering: Fasenra er beregnet til langtidsbehandling. Behovet for fortsatt behandling bør vurderes minst én gang årlig, basert på sykdommens alvorlighetsgrad, graden av sykdomskontroll og eosinofiltall i blod.
Astma: Anbefalt dose er 30 mg som subkutan injeksjon hver 4. uke for de første 3 dosene, og deretter hver 8. uke. Behandlingen skal startes opp av lege med erfaring med diagnostisering og behandling av alvorlig astma.
EGPA: Anbefalt dose er 30 mg som subkutan injeksjon hver 4. uke. Hos pasienter som utvikler livstruende manifestasjoner av EGPA, skal behovet for fortsatt behandling vurderes, siden Fasenra ikke har blitt undersøkt i denne populasjonen.
Kontraindikasjoner: Overfølsomhet overfor virkestoffet eller overfor noen av hjelpestoffene.
Vanlige bivirkninger: Feber, reaksjon på injeksjonsstedet, overfølsomhetsreaksjon, faryngitt, hodepine.
Ukjent frekvens: Anafylaktisk reaksjon.
Forsiktighetsregler: Skal ikke brukes ved akutt forverring av astma. Pasienten bør instrueres om å søke medisinsk hjelp dersom astmaen forblir ukontrollert eller forverres. Bruk bør unngås under graviditet og amming.
Pakninger og priser: Injeksjonsvæske, oppløsning i ferdigfylt penn (30 mg): 1 stk. kr 34065,90. Injeksjonsvæske, oppløsning i ferdigfylt sprøyte (30 mg): 1 stk. kr 34065,90.
Reseptgruppe: C. Refusjon: Alvorlig astma. H-resept. Refusjonsberettiget bruk: Der det er utarbeidet nasjonale handlingsprogrammer/nasjonal faglig retningslinje og/eller anbefalinger fra RHF/LIS spesialistgruppe skal rekvirering gjøres i tråd med disse. Vilkår: 216 Refusjon ytes kun etter resept fra sykehuslege eller avtalespesialist. Fasenra inngår i RHF anbefalinger for alvorlig ukontrollert T2-høy astma.
For fullstendig informasjon, les mer på www.felleskatalogen.no
AstraZeneca AS - www.astrazeneca.no – P. box 6050 Etterstad - 0601 Oslo
ID: NO-14145-05-2025-FA
Norsk forening for Lungemedisin (2019) Praktisk veileder for alvorlig astma. Hentet 24. juni 2024 fra https://www.legeforeningen.no/contentassets/9768b9ea8ed94cfaa89598e18fb2945b/praktisk-veileder-for-alvorlig-astma-hos-voksne.pdf.
Heaney LG, de Llano LP, Al-Ahmad M et al. Eosinophilic and Noneosinophilic Asthma. Chest 2021;160:814-30.
Hogan SP, Rosenberg HF, Moqbel R et al. Eosinophils: biological properties and role in health and disease. Clin Exp Allergy 2008;38:709-50.
Jacobsen EA, Jackson DJ, Heffler E et al. Eosinophil Knockout Humans: Uncovering the Role of Eosinophils Through Eosinophil-Directed Biological Therapies. Annu Rev Immunol 2021;39:719-57.
McBrien CN, Menzies-Gow A. The Biology of eosinophils and Their Role in Asthma Front Med 2017;4:1-14.
Zeiger RS, Schatz M, Dalal AA et al. Blood Eosinophil Count and Outcomes in SevereUncontrolled Asthma: A Prospective Study. JACI Pract 2017;5:144-53.
Zeiger RS, Schatz M, Dalal AA et al . Utilization and Costs of Severe Uncontrolled Asthma in a Managed-Care Setting JACI Pract 2016;4:120-29.
Korn S, Bourdin A, Chupp G et al Integrated Safety and Efficacy Among Patients Receiving Benralizumab for Up to 5 Years. JACI Pract 2021;9:4381-92.
Fasenra SPC 4.1, 4.2, 4.8, 5.1.
Bleecker ER, FitzGerald JM, Chanez P, et al. Efficacy and safety of benralizumab for patients with severe asthma uncontrolled with high-dosage inhaled corticosteroids and long-acting β2-agonist(SIROCCO): a randomised, multicentre, placebo-controlled phase 3 trial. Lancet 2016;388:2115–27.
Nair P, Wenzel S, Rabe K et al. Oral Glucocorticoid–Sparing Effect of Benralizumab in Severe Asthma. N Engl J Med 2017;376:2448-58.