Hold deg oppdatert!
Få relevant informasjon om blant annet:
- Medisinske nyheter
- Webinarer
- Pasientstøtte
- Produktinformasjon
- Bivirkningsrapportering
Du kan når som helst trekke tilbake ditt samtykke.

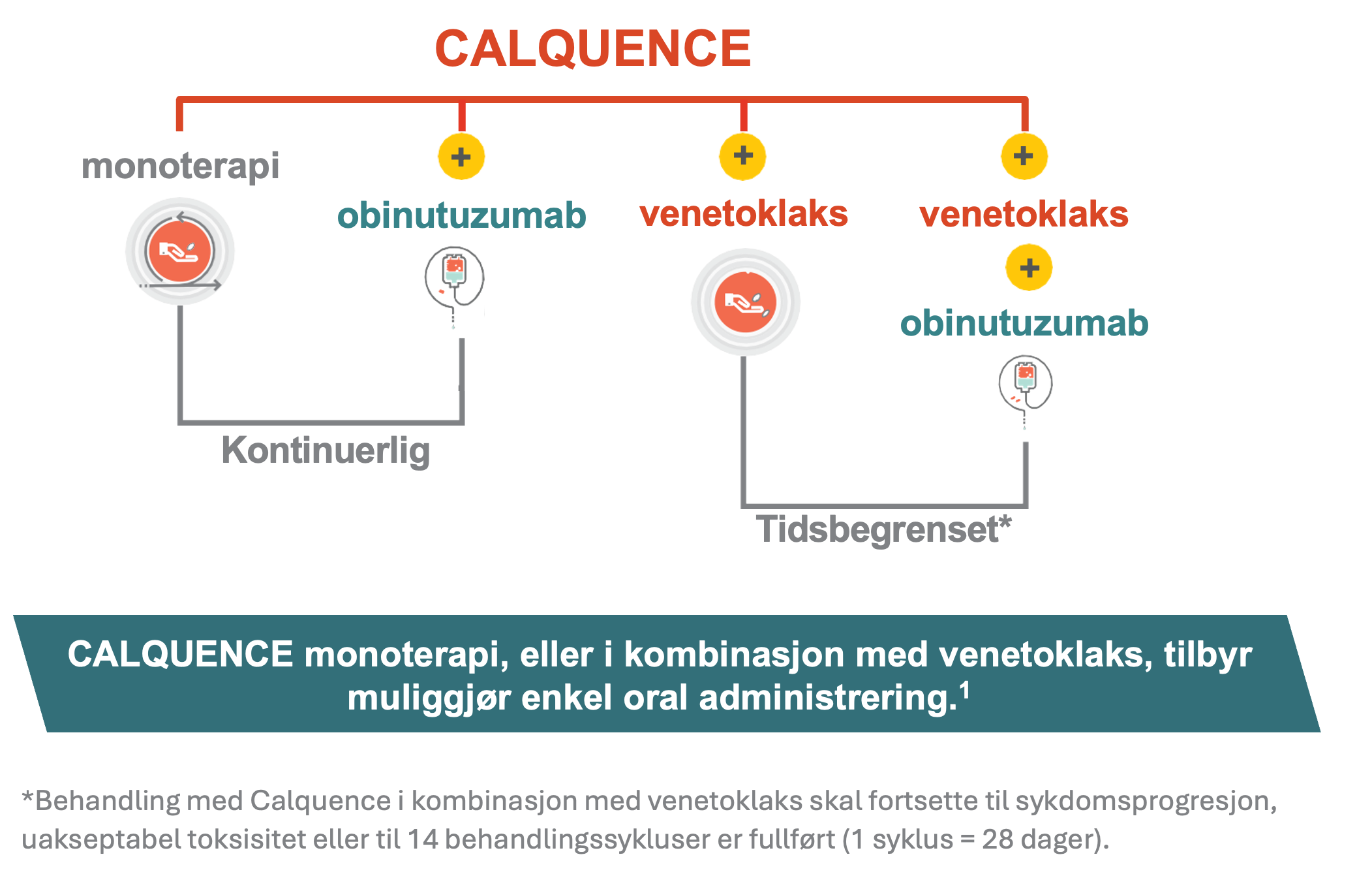
Calquence er en selektiv Brutons tyrosinkinase (BTK)-hemmer, som tas oralt to ganger daglig. Calquence binder seg til BTK og hemmer tumorcellesignalering via B-cellereseptoren.1
*H-resept finansiering kun etter resept fra sykehuslege eller avtalespesialist. Calquence inngår i Helseforetakenes anbefaling for onkologiske legemidler og rekvirering skal gjøres i tråd med disse: https://www.sykehusinnkjop.no/avtaler-legemidler/onkologi

Calquence i kombinasjon med venetoklaks, med eller uten obinutuzumab vs. FCR/BR hos pasienter med tidligere ubehandlet KLL i en randomisert, åpen fase III-studie.3
Les AMPLIFY-studien
Calquence med eller uten obinutuzumab vs. obinutuzumab pluss klorambucil hos pasienter med behandlingsnaiv KLL i en åpen, randomisert fase III-studie.4
Les ELEVATE-TN-studien
Calquence vs. IdR/BR hos pasienter med relapse eller refraktær KLL som hadde fått minst én tidligere behandling. Pasientene fikk enten Calquence-monoterapi eller utprøvers valg av standardbehandling i en åpen, randomisert fase 3-studie.5
Les ASCEND-studienHer har vi samlet tidligere episoder av AstraZenecas podkastserie «The Hematology Podcast». Her inviteres interessante gjester til å diskutere aktuelle temaer innen hematologi, med fokus på kronisk lymfatisk leukemi (KLL).
Du kan enkelt bli abonnent ved å klikke på lenken
Lytt til The Hematology PodcastHer har vi samlet filmer der eksperter innen ulike felt relatert til kronisk lymfatisk leukemi gir svar på aktuelle spørsmål.
Se Webinars and Expert AnswersBesøk nettbutikken vår for å bestille pasientbrosjyrer og studier med Calquence (akalabrutinib).
Bestill materialeIndikasjoner: Som monoterapi, eller i kombinasjon med obinutuzumab, til behandling av voksne pasienter med tidligere ubehandlet kronisk lymfatisk leukemi (KLL). Som monoterapi til behandling av voksne pasienter med KLL som har fått minst én tidligere behandling. I kombinasjon med venetoklaks med eller uten obinutuzumab til behandling av voksne pasienter med tidligere ubehandlet KLL. I kombinasjon med bendamustin og rituksimab (BR) til behandling av voksne pasienter med tidligere ubehandlet mantelcellelymfom (MCL) som ikke er kvalifiserte for autolog stamcelletransplantasjon (ASCT). Som monoterapi til behandling av voksne pasienter med residiverende eller refraktær MCL som ikke tidligere har fått behandling med en BTK-hemmer.
Dosering: Behandling med dette legemidlet skal igangsettes og følges opp av lege med erfaring i bruk av legemidler mot kreft.
Voksne: Anbefalt dose som monoterapi eller i kombinasjon er 100 mg 2 ganger daglig. Behandling bør fortsette inntil sykdomsprogresjon, uakseptabel toksisitet eller til det er fullført 14 behandlingssykluser (hver syklus er på 28 dager) når kombinert med venetoklaks.
Forsiktighetsregler: Alvorlige blødninger, inkl. blødning i CNS og gastrointestinal blødning er sett. Pasienter som bruker antitrombotiske midler kan ha økt risiko for blødning og forsiktighet skal utvises ved bruk. Warfarin eller andre vitamin K-antagonister skal ikke gis samtidig med akalabrutinib. Atrieflimmer/flutter forekom hos pasienter med hematologiske maligniteter både ved monoterapi og i kombinasjon med obinutuzumab. Overvåk for symptomer på atrieflimmer og atrieflutter og foreta EKG om nødvendig. Ved høy risiko for tromboembolisk sykdom, skal nøye kontrollert behandling med antikoagulanter og andre behandlingsalternativer vurderes. Tumorlysesyndrom (TLS) har blitt rapportert ved behandling med (akalabrutinib). Pasienter som anses å ha risiko for TLS (f.eks. med stor tumormasse ved baseline) bør vurderes for mulig risiko for TLS og overvåkes nøye som klinisk indisert.
Interaksjoner: Samtidig bruk av sterke CYP3A-hemmere eller CYP3A-induktorer skal unngås; kan gi hhv. økt og redusert eksponering for akalabrutinib.
Bivirkninger: Monoterapi: Vanligste bivirkninger (≥ 20 %): Infeksjon, diaré, hodepine, muskel- og skjelettsmerter, blåmerker, hoste, artralgi, fatigue, kvalme og utslett.
Kombinasjonsbehandling: Vanligste bivirkninger (≥ 20 %): Infeksjon, muskel- og skjelettsmerter, diaré, hodepine, blåmerker, leukopeni, nøytropeni, trombocytopeni, anemi, hoste, fatigue, artralgi, kvalme, utslett, svimmelhet, oppkast og forstoppelse.
Pakninger og priser: 60 stk. (blister) kr 69.842,20. Reseptgruppe C.
For mer info om Calquence, se www.felleskatalogen.no eller godkjent SPC.
NO-14484-08-25-ONC
Calquence® (acalabrutinib), Summary of Product Characteristics, www.ema.europa.eu
Beslutningsforum for Nye Metoder ID2020_037, ID2021_086, ID2021_087, ID2024_073; nyemetoder.no/sok/?q=akalabrutinib
Brown J. N Engl J Med. 2025;392(8):748-762
Sharman P. et al. Blood. 2025. blood.2024024476
Ghia et al. Hemasphere. 2022; 6 (12):e801